
【题目】已知锌及其化合物的性质与铝及其化合物的性质相似。现向ZnCl2溶液中逐渐滴加NaOH溶液,溶液的PH与某些离子的浓度关系如图(横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-的物质的量浓度的对数;假设Zn2+的浓度为10-5mol/L时,已沉淀完全)。则下列说法不正确的是

A. 某废液中含Zn2+,沉淀对Zn2+以控制溶液pH的范围是(8,12 ) ,
B. 往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:Zn2++4OH-=[Zn(OH)4]2-
C. 向1L 0.01mol/LZnCl2溶液中逐渐滴加NaOH溶液,当PH>6时Zn2+开始沉淀
D. 向1L 0.01mol/LZnCl2溶液中逐渐滴加NaOH溶液至PH=7,此时溶液中Zn2+的浓度为10-3mol/L
【答案】C
【解析】A、根据题中pH与浓度的关系,Zn2+转化沉淀,需要控制溶液的pH在8~12之间,故A说法正确;B、根据pH与浓度的关系,当pH大于12时,锌元素以[Zn(OH)4]2-,因此离子反应方程式为Zn2++4OH-=[Zn(OH)4]2-,故B说法正确;C、当pH=8时,沉淀完全,此时溶液中c(Zn2+)=10-5mol·L-1,即Ksp=10-5×(10-6)2=10-17,当c(Zn2+)=0.01mol·L-1时,c(OH-)2=10-17/0.01mol·L-1=10-15mol·L-1,因此c(OH-)=10-7.5mol·L-1, pOH=7.5,即pH=14-7.5=6.5,即当pH>6.5时,开始出现沉淀,故C说法错误;D、根据C选项得到的Ksp,当pH=7时,溶液中c(Zn2+)=Ksp/c2(OH-)=10-17/(10-7)2=10-3mol·L-1,故D正确。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率为( )
4NO(g)+6H2O(g),在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率为( )
A. v(O2)=0.01 mol/(L·s) B. v(NO)=0.008 mol/(L·s)
C. v(H2O)=0.003 mol/(L·s) D. v(NH3)=0.004 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一,铁及其化合物在现代社会各个领域仍有广泛的应用。
I.氧化物—Fe2O3:用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)制取高纯铁红,实验室常用萃取剂X(甲基异丁基甲酮)萃取法制取高纯铁红的主要实验步骤如下:

已知:HCl(浓) + FeCl3![]() HFeCl4 。试回答下列问题:
HFeCl4 。试回答下列问题:
(1)用萃取剂X萃取,该步骤中:
① Ca2+、Mn2+、Cu2+等杂质离子主要在__________(填“水”或“有机”)相。
② 若实验时共用萃取剂X 150mL,萃取率最高的方法是__________(填字母)。
a.一次性萃取,150mL b.分2次萃取,每次75mL c.分3次萃取,每次50mL
(2)用高纯水反萃取,萃取后水相中铁的存在形式是________________(写化学式);反萃取能发生的原因是___________________。
(3)所得草酸铁沉淀需用冰水洗涤,其目的一是洗去沉淀表面吸附的杂质离子,二是________________。
(4)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定,已知铬的还原产物为Cr3+,写出该滴定反应的离子方程式 ___________________。
II.含氧酸盐—铁酸铜(CuFe2O4)是很有前景的热化学分解水制氢的材料,CuFe2O4在制氢过程中可以循环使用。在热化学循环分解水制氢的过程中,铁酸铜(CuFe2O4)先要煅烧成氧缺位体(CuFe2O4-a),氧缺位值(a)越大,活性越高,制氢越容易。
(5)根据以上提示,写出氧缺位体与水常温下反应制氢的化学方程式____________。
(6)课外小组将铁酸铜样品在N2的气氛中充分煅烧,得氧缺位体的质量为原质量的96.6%,则氧缺位值(a)=__________。(结果保留小数点后2位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.用氢氟酸对玻璃进行刻蚀可制成赏心悦目的雕花玻璃
B.Na2CO3粉末遇水生成含有结晶水的碳酸钠晶体,该晶体一定是Na2CO310H2O
C.氯水和干燥的氯气均能使鲜花褪色
D.合金的硬度可以大于它的纯金属部分,合金的熔点也可以低于它的成分金属
查看答案和解析>>
科目:高中化学 来源: 题型:
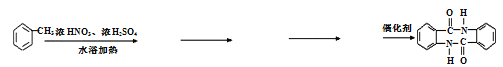
【题目】甲苯可用于合成治疗粘膜溃疡、创面等的镇痛药物苯佐卡因及食用香料F,其合成路线如下:
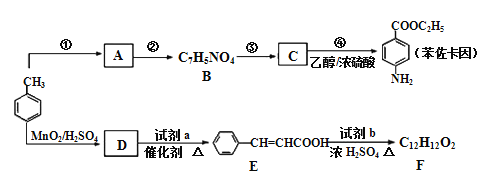
已知:
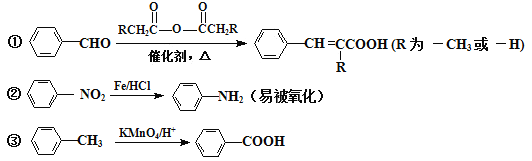
④苯环上发生取代反应规律:当苯环碳原子连有甲基时,主要在其邻位或对位上引入官能团;当苯环碳原子连有羧基时,主要在其间位上引入官能团。
请回答下列问题:
(1)B分子中含氧官能团的名称是_______;试剂a的结构简式为________。
(2)下列关于苯佐卡因合成路线的说法中错误的是________(填字母)
a.步骤①和②可以互换
b. 反应①、④属于取代反应
c.反应①的条件为酸性高锰酸钾溶液
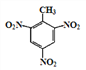
d.反应①除主要生成A外,还可能生成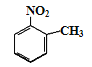 、
、
(3)质谱图显示试剂b的相对分子质量为58,分子中不含甲基,且为链状结构,b的化学名称是______,写出E与试剂b生成F的化学方程式__________。
(4)E有多种同分异构体,符合下列条件的有________种。
①苯环上有三个取代基;②能发生银镜反应,且1 mol该有机物生成4 mol Ag
写出其中一种核磁共振氢谱有4组吸收峰,且峰面积之比为1∶2∶2∶3的有机物的结构简式___________。
(5)参照上述合成路线及信息,根据已有知识,完善下列以甲苯为主要原料制备有机物(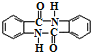 )的合成路线_________(无机试剂任选)。
)的合成路线_________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明酸性溶液中,能共存的离子组是
A.NH4+、OH-、Al3+、Cl- B.K+、SO42-、HCO3-、Na+
C.Mg2+、NO3-、Cl-、Na+ D.MnO4-、K+、SO42-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
A. 容器内的总压强不随时间变化
B. 断裂4molH—O键的同时,断裂4molH—H键
C. 混合气体的平均相对分子质量不变
D. 反应不再进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按图所示工艺流程进行生产,可制得轻质氧化镁(轻质体积蓬松,体积是等质量的重质氧化镁的三倍)。

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表l 生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.l |
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。表2原料价格表
物质 | 价格/元 吨-1 |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
(1)为了加快卤块的溶解,我们可以选择那些方法_______(请写出两种方法);
(2)在步骤②中加入的试剂X,最佳的选择是________,在酸性条件下,其对应的离子方程式是________________
(3)在步骤③中加入的试剂应是________;之所以要控制pH=9.8,其目的是__________
(4)在步骤④中加入的试剂Z应是___________;
(5)在步骤⑤中发生的反应是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。已知:甲醇的燃烧热486为kJ·mol-1 ( 2CO (g) + O2(g) = 2CO2(g) △H b =-566.0 kJ·mol-1)
试写出CH3OH(l)在氧气中完全燃烧生成CO和H2O(l)的热化学方程式: 。
(2)常温下某溶液中由水电离的c(H+)=10-10 mol/L,则该溶液的pH为 _______。
(3)常温下,向V L pH=12的Ba(OH)2溶液中逐滴加入一定浓度的NaHSO4稀溶液,当溶液中的Ba2+恰好沉淀完全时,溶液pH=11。则Ba(OH)2溶液与NaHSO4溶液的体积比为__________,NaHSO4溶液的物质的量浓度为 。
(4)常温下,0.5mol/L的NH4Cl溶液的为pH=5.该溶液显酸性的原因是(用离子方程式表示) 。计算常温下氨水的电离平衡常数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com