
| A. | CO2 | B. | Ca(OH)2 | C. | H2O | D. | CaO |
分析 氧化物是指由两种元素组成,一种元素是氧元素的化合物属于氧化物,酸性氧化物是和碱反应生成盐和水的氧化物,碱性氧化物是能和酸反应生成盐和水的氧化物.
解答 解:A.二氧化碳能和碱性氧化物反应生成盐,本身属于属于酸性氧化物,与其它酸性氧化物不反应,故A错误;
B.Ca(OH)2由钙、氢、氧三种元素组成,不属于氧化物,属于二元强碱,故B错误;
C.水能和酸性氧化物反应,如与二氧化硫反应生成亚硫酸,也能与碱性氧化物反应,如与氧化钠反应生成氢氧化钠,本身属于氧化物,故C正确;
D.CaO能和酸性氧化物反应,本身属于碱性氧化物,与其它碱性氧化物不反应,故D错误.
故选C.
点评 本题考查学生酸性氧化物、碱性氧化物的概念应用,注意题干的条件,符合题意的物质需满足三个条件,缺一不可,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10% | B. | 34% | C. | 72% | D. | 17% |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
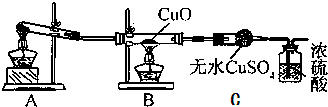
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 锗是一种金属性很强的元素 | B. | 锗的单质具有半导体的性能 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗酸(H4GeO4)是难溶于水的弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2+4H++4e-=2H2O | B. | O2+2H2O+4e-=4OH- | ||
| C. | N2H4+4OH--4e-=N2+4H2O | D. | N2H4+4H++2e-=2NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com