
 CO2(g)+H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t1��t2)��
CO2(g)+H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t1��t2)��| ��Ӧʱ��/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ʵ���� | ��Ӧ�� | ���� |
| �� | 10 mL 2%H2O2��Һ | �� |
| �� | 10 mL 5%H2O2��Һ | �� |
| �� | 10 mL 5%H2O2��Һ | 1 mL 0.1 mol��L��1FeCl3��Һ |
| �� | 10 mL 5%H2O2��Һ������HCl��Һ | 1 mL 0.1 mol��L��1FeCl3��Һ |
| �� | 10 mL 5%H2O2��Һ������NaOH��Һ | 1 mL 0.1 mol��L��1FeCl3��Һ |
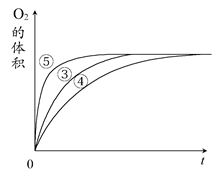
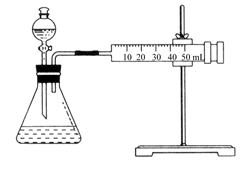
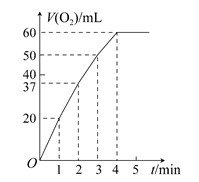
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��9mol����L��s����1 | B��27mol����L��s����1 |
| C��81mol����L��s����1 | D��243mol����L��s����1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)��D(g)����2 min��B��Ũ�ȼ���0.6 mol/L���Դ˷�Ӧ���ʵı�ʾ��ȷ����(����)
2C(g)��D(g)����2 min��B��Ũ�ȼ���0.6 mol/L���Դ˷�Ӧ���ʵı�ʾ��ȷ����(����)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4NO��6H2O������Ӧ���ʷֱ���v��NH3����v��O2����v��NO����v��H2O����ʾ����������ȷ�Ĺ�ϵ�� ����������
4NO��6H2O������Ӧ���ʷֱ���v��NH3����v��O2����v��NO����v��H2O����ʾ����������ȷ�Ĺ�ϵ�� ����������A�� v��NH3����v��O2�� v��NH3����v��O2�� |
B��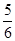 v��O2����v��H2O�� v��O2����v��H2O�� |
C��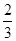 v��NH3����v��H2O�� v��NH3����v��H2O�� |
D�� v��O2����v��NO�� v��O2����v��NO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO(g) + H2O(g) ��H1����41.2kJ��moL��1��
CO(g) + H2O(g) ��H1����41.2kJ��moL��1�� CH3OH(g) + H2O(g) ��H2����49kJ��moL��1��
CH3OH(g) + H2O(g) ��H2����49kJ��moL��1��| �¶� | ת���ʣ�%�� | ���ʵ�����mol�� | ||
| H2 | CO2 | CH3OH | CO | |
| 240�� | | 10 | 0.05 | 0.05 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol/L��H2��Ũ��Ϊ5 mol/L��3 min����NH3Ũ��Ϊ0.6 mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����
2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol/L��H2��Ũ��Ϊ5 mol/L��3 min����NH3Ũ��Ϊ0.6 mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ���� | A��v(NH3)="0.2" mol/��L��s�� | B��v(N2)="1.0" mol/��L��min�� |
| C��v(H2)="1.67" mol/��L��min�� | D��v(H2)="0.3" mol/��L��min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ?2AB3��Ӧ��˵�����·�Ӧ���ʱ�ʾ��Ӧ�����ǣ� ��
?2AB3��Ӧ��˵�����·�Ӧ���ʱ�ʾ��Ӧ�����ǣ� ��| A��v(AB3)��0.5 mol/(L��min) | B��v(B2)��0.6 mol/(L��min) |
| C��v(A2)��0.4 mol/(L��min) | D�����ж� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com