
燃烧电池是燃料(如CO、H2、CH4等)跟氧气(或空气)起反应将化学能转化为电能的装置,电解质溶液是强碱(如KOH)溶液,下面关于甲烷燃烧电池的说法不正确的是
A.正极反应式为O2+2H2O+4e—=4OH—
B.负极反应式为CH4+10OH——8e—=CO32—+7H2O
C.随着放电的进行,溶液的pH值不变
D.甲烷燃烧电池的能量利用率比甲烷燃烧的大
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2010年海南省高二上学期第二次月考化学试卷 题型:选择题
燃料电池是燃料(如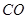 、
、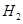 、
、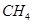 )等跟
)等跟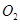 (或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如
(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如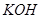 )溶液,下列关于甲烷燃料电池的说法中不正确的是:
)溶液,下列关于甲烷燃料电池的说法中不正确的是:
A、负极的电极反应式为: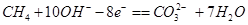
B、通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应
C、随着反应的进行,电解质溶液的pH保持不变
D、甲烷燃料电池的能量利用率比甲烷燃烧的大
查看答案和解析>>
科目:高中化学 来源:海南省期末题 题型:不定项选择题
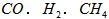 )等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如
)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如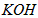 )溶液,下列关于甲烷燃料电池的说法中不正确的是
)溶液,下列关于甲烷燃料电池的说法中不正确的是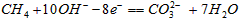
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池是燃料(如![]() 、
、![]() 、
、![]() )等跟
)等跟![]() (或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如
(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如![]() )溶液,下列关于甲烷燃料电池的说法中不正确的是:
)溶液,下列关于甲烷燃料电池的说法中不正确的是:
A、负极的电极反应式为:![]()
B、通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应
C、随着反应的进行,电解质溶液的pH保持不变
D、甲烷燃料电池的能量利用率比甲烷燃烧的大
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池是燃料(如![]() 、
、![]() 、
、![]() )等跟
)等跟![]() (或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如
(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如![]() )溶液,下列关于甲烷燃料电池的说法中不正确的是:
)溶液,下列关于甲烷燃料电池的说法中不正确的是:
A、负极的电极反应式为:![]()
B、通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应
C、随着反应的进行,电解质溶液的pH保持不变
D、甲烷燃料电池的能量利用率比甲烷燃烧的大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com