
| A.①②⑤ | B.①②④⑤ | C.①②④⑤⑦ | D.①②⑤⑦ |
科目:高中化学 来源:不详 题型:单选题
| A.在容量瓶中加一定体积的水,再加入浓硫酸以配制准确浓度的稀硫酸 |
| B.用溶解、过滤、蒸发的实验操作分离硝酸钾与氯化钠的混合物 |
| C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D.加入适量硫酸以除去硫酸钠中的少量碳酸钠杂质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解质和非电解质一定都是化合物 |
| B.我们把微粒大小在1nm~100nm的粒子称为胶体 |
| C.量筒的“0”刻度在下,而滴定管的“0”刻度在上 |
| D.试管、坩埚、蒸发皿均是可以直接加热的玻璃仪器 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
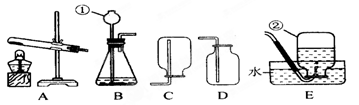
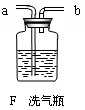
| A.NaHCO3溶液, | B.NaOH溶液, | C.澄清石灰水, | D.浓硫酸)写出洗气过程中反应的化学方程式____________________________________。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将氯化镁溶液直接蒸发至干,可获得纯净的无水MgCl2固体 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.用KSCN溶液检验硫酸亚铁溶液是否氧化变质 |
| D.用苯萃取溴的四氯化碳溶液中的溴 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 物质 | SiCl4 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | — | 315 | — |
| 熔点/℃ | -70.0 | — | — | — |
| 升华温度/℃ | — | 180 | 300 | 162 |
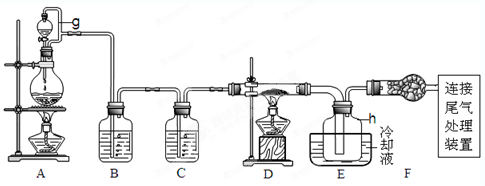
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用pH试纸测定某一溶液的pH时,将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 |
| B.过滤时,漏斗里液体的液面要高于滤纸的边缘 |
| C.胶头滴管的管口直接伸入试管里滴加液体,以免外溅 |
| D.实验室取用液体药品做实验时,如没有说明用量,一般取1~2 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2KNO2+O2↑,
2KNO2+O2↑,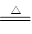 2CuO+2NO2↑+O2↑,4AgNO3
2CuO+2NO2↑+O2↑,4AgNO3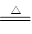 4Ag+4NO2↑+O2↑
4Ag+4NO2↑+O2↑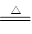 M(NO2)2+O2↑
M(NO2)2+O2↑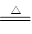 2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com