
【题目】A、B、C、D、E均为短周期元素,且原子序数依次递增。A、E同主族,B、D同周期,且B和D最外层电子数之和为10;A与D可形成A2D、A2D2共价化合物。请回答下列问题。
(1)D位于周期表第_____________周期第_____________族;
(2)E离子的结构示意图为_____________;与E同周期的元素中,金属性最弱的金属元素名称是___________,最稳定的气态氢化物的化学式为_____________;
(3)C2的电子式为_____________,B与D通常能形成_____________(填“离子”或“共价”)化合物,在E2D2中含有的化学键有__________________________。
【答案】 二 ⅥA ![]() 铝 HCl
铝 HCl ![]() 共价 离子键、非极性共价键
共价 离子键、非极性共价键
【解析】A、B、C、D、E均为短周期元素,且原子序数依次递增.A与D可形成A2D、A2D2共价化合物,则A为H元素、D为O元素;B、D同周期,且B和D最外层电子数之和为10,则B为碳元素;C的原子序数介于碳、氧之间,故C为N元素;A、E同主族,E的原子序数大于氧,故E为Na;
(1)D为O元素,位于周期表第二周期ⅥA族;
(2)E离子为Na+,Na+的结构示意图为![]() ;与E同周期的元素中,金属性最弱的金属元素名称是铝,所形成的最稳定的气态氢化物的化学式为HCl;
;与E同周期的元素中,金属性最弱的金属元素名称是铝,所形成的最稳定的气态氢化物的化学式为HCl;
(3)N2的电子式为![]() ,B与D通常能形成CO、CO2,属于共价化合物,在Na2O2中含有的化学键有离子键、非极性共价键。
,B与D通常能形成CO、CO2,属于共价化合物,在Na2O2中含有的化学键有离子键、非极性共价键。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】在恒温条件下,可逆反应H2(g)+I2( g)2HI(g)在体积固定的密闭容器中进行,达到平衡的标志是( )
A. 混合气体的颜色不再改变B. H2、I2、HI分子个数比为1:1:2
C. 混合气体中I2和H2的体积分数相等D. 混合气体的压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A. 标准状况下,16g的甲醇所含的质子数等于10NA
B. 标准状况下,22.4 L己烷中共价键数目为19NA
C. 1 mol苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA
D. 0.3 mol AgNO3受热完全分解(2AgNO3===2Ag+2NO2↑+O2↑),用排水法收集到气体的分子数为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且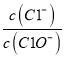 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
A. 某温度下,若反应后溶液中n(ClO-)=1mol ,n(C1O3-)=2mol,则n(C1-)= 11 mol
B. 参加反应的氯气的物质的量等于0.5amol
C. 上述反应中转移电子的物质的量至少为0.5amol
D. 改变温度,产物中KC1O3的最大理论产量为![]() amol
amol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO·Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是______________________________________________。
(2)NaOH溶液可以除去铝表面的氧化膜,在处理过程中常会产生H2,产生H2的离子方程式是__________________________________________。
(3)工业上以铝土矿(Al2O3·H2O)为原料生产铝,主要包括下列过程:
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH)3固体;
iii.使Al(OH)3脱水生成Al2O3;
iv.电解熔融Al2O3生成Al。
铝土矿粉粹的目的是________________________,电解熔融Al2O3时,加入冰晶石,其作用是__________________________。写出电解熔融Al2O3的化学方程式__________________________________________________。
(4)明矾化学式为KAl(SO4)2·12H2O,向明矾溶液中加入Ba(OH)2溶液,当溶液中的SO42-恰好沉淀时,铝元素的存在形式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物9,10-二甲基菲的结构如图所示,下列关于该物质的说法正确的是

A. 该物质分子式为C16H12
B. 该物质与甲苯互为同系物
C. 该物质能与溴水发生取代反应和加成反应
D. 该物质苯环上七氯代物的同分异构体有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①可以用Cu(OH)2悬浊液用一种试剂鉴别甲酸、乙酸、乙醛、乙醇。
②可用酸性K2Cr2O7溶液检验是否酒后驾车,该应用利用了乙醇的还原性和低沸点的性质。
③向银氨溶液中加入几滴乙醛后用酒精灯加热至沸腾制可得银镜。
④向足量的浓苯酚溶液中滴入少量溴水,可观察到有白色沉淀生成,该沉淀为2,4,6-三溴苯酚。
⑤该分子 中的碳原子可能都在同一平面。
中的碳原子可能都在同一平面。
⑥做过银镜反应实验后的试管,用氨水洗涤。
A. ①②④⑤⑥ B. ①②③④ C. ①②④ D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
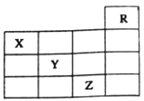
① X 的气态氢化物与Y最高价氧化物对应的水化物的溶液能发生反应生成盐
② 同浓度的Y、Z的气态氢化物的水溶液的酸性Y<Z
③ Z的单质常温下是深红棕色液体,具有氧化性
④ Z 的原子序教比Y大19
⑤ Z 所在的周期中含有32种元素
A. 只有③ B. 只有①④ C. 只有①②③④ D. ①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com