
能正确表示下列反应的离子方程式是
A.Na2O2与H2O反应:Na2O2+H2O=2Na++2OH-+O2↑
B.硫酸铝与过量氨水反应:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
C.NO2溶于水:3NO2+H2O=2H++2NO3-+NO
D.用FeCl3溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
下列说法中,不正确的是
A.原子最外层电子数比次外层电子数多的元素一定位于第周期
B.从氟到碘,单质与氢气发生化合反应越来越难
C.14C和14N两种核素的质量数相同,中子数也相同
D.离子化合物中可能含有共价键,但共价化合物中一定不含离子健
查看答案和解析>>
科目:高中化学 来源: 题型:
在固定体积的容器内进行反应2HI(g) 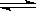 H2(g) + I2(g),达到平衡状态的标志是
H2(g) + I2(g),达到平衡状态的标志是
A.I2(g)的消耗速率等于H2的消耗速率
B.容器中各组分的浓度不随时间变化
C.容器内气体的压强不再变化
D.单位时间内生成n mol H2,同时生成n mol HI
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)铅蓄电池的电池总反应式为:
Pb+PbO2+4H++2SO42- 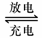 2PbSO4+2H2O回答下列
2PbSO4+2H2O回答下列
问题。(不考虑氢、氧的氧化还原)
①放电时:负极的电极反应式是 ,
电解液中H2SO4的浓度将变________,当外电路通过
2mol电子时,理论上负极板的质量增加 g。
②在完全放电耗尽PbO2和Pb时,将原Pb和PbO2极板
按右图连接,电解一段时间后,则在A电极上生成 __________,B电极上?生成________。
(2)三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是
a.可用铁作阳极材料
b.电解过程中阳极附近溶液的pH升高
c.阳极反应方程式为:2Cl--2e-=Cl2↑
d.1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.将SO2通入BaCl2溶液中至饱和,将产生白色沉淀
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
C.浓HNO3 、氯水、AgBr固体、AgNO3溶液都应该保存在棕色玻璃瓶中
D.工业上分别用电解融熔NaCl、MgCl2、AlCl3的方法制得金属Na、Mg、Al
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液可能存在Al3+、H+、Na+、SO32-、CO32-、NO3-、AlO2-和S2-八种离子中的几种,进行如下实验:①向溶液中加入足量的稀盐酸,产生无色气体;②继续滴加BaCl2溶液,产生白色沉淀;③过滤后,向滤液中逐滴加入NaOH溶液,产生白色沉淀;继续滴加,白色沉淀消失。由此推断原溶液中 ( )
A.一定存在的离子是Na+、SO32-、CO32-、AlO2-
B.可能存在的离子是Al3+、CO32-
C.一定存在的离子是Na+、SO32-、NO3-、AlO2-
D.可能存在的离子是CO32- 、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中,既能与强酸又能与强碱反应的是
①Na2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3
A.①②③④ B.①②③ C.①②④ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
A.Na2CO3是碱 B.Na2CO3是盐
C.Na2CO3是钠盐 D.Na2CO3是碳酸盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com