
| A、电解饱和NaCl溶液来制备钠 |
| B、电解熔融AlCl3晶体来制备铝 |
| C、用焦炭在高温下还原二氧化硅来制备硅 |
| D、用黄铜矿(CuFeS2)直接电解精炼来制备铜 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、反应①的反应热为221kJ |
| B、碳的燃烧热为△H=-221kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为△H=-57.3kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、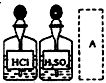 |
B、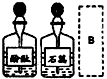 |
C、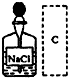 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、聚四氟乙烯的结构简式: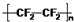 | ||
B、Na2O2的电子式: | ||
C、
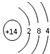 | ||
D、丙烷的分子球棍模型示意图: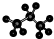 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何化学反应都伴随有能量变化 |
| B、△H>0表示放热反应,△H<0表示吸热反应 |
| C、化学键的断裂会放出能量 |
| D、反应物总能量比生成物总能量高的反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com