
【题目】Ⅰ.已知NH3H2O与醋酸的电离度在同温同浓度下相等。向少量Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,结果固体完全溶解。
甲同学的解释是:
Mg(OH)2 (固)![]() Mg2++2OH- (1)
Mg2++2OH- (1)
NH4++H2O![]() NH3H2O+H+ (2)
NH3H2O+H+ (2)
H++OH-![]() H2O (3)
H2O (3)
由于(3)的发生,使平衡(1)右移,沉淀溶解。
乙同学的解释是:
Mg(OH)2 (固)![]() Mg2++2OH- (1)
Mg2++2OH- (1)
NH4Cl=NH4++Cl- (2)
NH4++OH-![]() NH3H2O (3)
NH3H2O (3)
由于(3)的发生,使平衡(1)右移,沉淀溶解。
丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确。
(1)他选用的试剂是__________(填写编号)。
A. NH4NO3 B. CH3COONH4 C. Na2CO3 D. NH3H2O
(2)实验步骤:____________________________;
(3)实验结论:____________________________。
Ⅱ.关于“电解氯化铜溶液时的pH变化”问题,化学界有两种不同的观点。
观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高;
观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时的pH的变化如图。请回答下列问题:
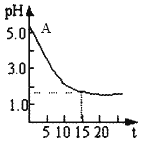
(1)用离子方程式表示电解前氯化铜溶液的pH处于A点的原因:______________。
(2)“理论派”所持观点的理论依据是:_______________________。
(3)你支持哪种观点:_________(理论派、实验派)。其理由是_____________。
【答案】B 向Mg(OH)2悬浊液中加入适量的饱和醋酸铵CH3COONH4溶液,振荡,观察Mg(OH)2是否溶解 若Mg(OH)2溶解,则乙同学的解释正确;若Mg(OH)2不溶解,则甲同学的解释正确 Cu2++2H2O![]() Cu(OH)2+2H+ 随着电解的进行,c(Cu2+)减少,水解平衡向逆方向移动,c(H+)下降,pH增大 实验派 电解时阳极产生的Cl2溶解生成HCl和HClO,使溶液c(H+)增大,pH减小
Cu(OH)2+2H+ 随着电解的进行,c(Cu2+)减少,水解平衡向逆方向移动,c(H+)下降,pH增大 实验派 电解时阳极产生的Cl2溶解生成HCl和HClO,使溶液c(H+)增大,pH减小
【解析】
I.为了证明Mg(OH)2悬浊液与氯化铵溶液的反应原理,可加入醋酸铵溶液检验,因醋酸铵溶液呈中性,如甲同学的解释正确,则氢氧化镁不溶解,如氢氧化镁溶解,则乙同学的解释正确,据此进行解答;
II.(1)根据盐的类型判断溶液的酸碱性;
(2)根据水解平衡的移动判断氢离子的浓度变化,从而判断pH值变化;
(3)根据电解生成物的性质判断溶液的酸碱性;
I.硝酸铵和氯化铵相似,只有铵根离子的水解,而碳酸钠和氨水溶液都呈碱性,只有CH3COONH4溶液显中性,可证明是否由于铵根离子水解呈酸性的原因导致氢氧化镁溶解,可以证明是甲合理还是乙合理,故合理选项是B;
(2)实验步骤:向Mg(OH)2悬浊液中加入适量的饱和醋酸铵CH3COONH4溶液,振荡,观察Mg(OH)2是否溶解;
(3)实验结论:若Mg(OH)2溶解,则乙同学的解释正确;若Mg(OH)2不溶解,则甲同学的解释正确;
II.(1)电解前氯化铜溶液pH=5,是由于氯化铜是强酸弱碱盐,溶于水,Cu2+能发生水解作用:Cu2++H2O![]() Cu(OH)2+2H+,当最终达到平衡时,溶液中氢离子浓度大于氢氧根离子浓度,所以溶液呈酸性pH<7;
Cu(OH)2+2H+,当最终达到平衡时,溶液中氢离子浓度大于氢氧根离子浓度,所以溶液呈酸性pH<7;
(2)随着电解的进行,溶液中Cu2+不断形成Cu(OH)2析出,溶液中铜离子浓度逐渐降低,使反应Cu2++H2O![]() Cu(OH)2+2H+向逆反应方向进行,c(H+)下降,溶液的pH增大;
Cu(OH)2+2H+向逆反应方向进行,c(H+)下降,溶液的pH增大;
(3)电解氯化铜生成氯气和铜,氯气易溶于水,与水反应生成盐酸和次氯酸,使溶液酸性增强,所以pH降低,所以我支持的观点是实验派。


科目:高中化学 来源: 题型:
【题目】有下列几种有机化合物的结构简式:(选填序号,下同)
①CH3CH═CH﹣CH2CH3 ② ③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥
③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥![]()
⑦CH3CH2CH2OCH3 ⑧![]() ⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
(1)互为同分异构体的是______________ (2)互为同系物的是___________
(3)官能团位置不同的同分异构体是_______ (4)官能团类型不同的同分异构体是__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活污水中氮是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180mg/L。
(1)写出NH4Cl电子式:___。
(2)氮原子的电子排布式是:___,写出与氯同周期,有2个未成对电子的原子的元素符号为___、___。
(3)为除去废水中的NH4+,向103L该污水中加入0.1mo1/LNaOH溶液,理论上需要NaOH溶液的体积为___L(计算结果保留两位小数)。
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目___。
___Fe+___NO3-+___H+→___Fe2++___NH4++___H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复旦大学王永刚的研究团队制得一种柔性水系锌电池,该可充电电池以锌盐溶液作为电解液,其原理如图所示。下列说法不正确的是
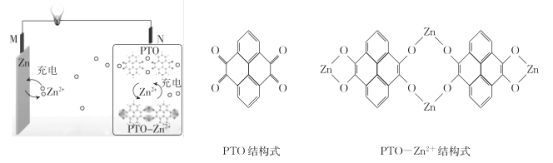
A.放电时,N极发生还原反应
B.充电时,Zn2+向M极移动
C.放电时,每生成1 mol PTO- Zn2+ ,M极溶解Zn的质量为260 g
D.充电时,N极的电极反应式为2PTO+8e- +4Zn2+=PTO- Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
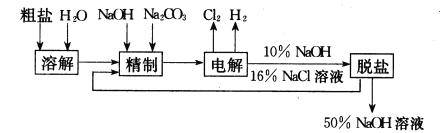
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应式为__________。 与电源负极相连的电极附近,溶液pH ________(选填:不变,升高或下降)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为___________,
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是______。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 _________。
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、_________(填写操作名称)除去NaCl。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 某有机物
某有机物![]() 与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重
与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重![]() 、
、![]() ;同温同压下,
;同温同压下,![]() 蒸气的密度是
蒸气的密度是![]() 的37倍。则能够与钠反应放出
的37倍。则能够与钠反应放出![]() 的
的![]() 的结构有(不考虑立体异构)( )
的结构有(不考虑立体异构)( )
A.6种B.5种C.4种D.3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B两种烃,已知A的分子式为C5Hm,而B的最简式为C5Hn(m、n均为正整数)。请回答下列问题:
(1)下列关于烃A和烃B的说法不正确的是 (填序号)。
a.烃A和烃B可能互为同系物
b.烃A和烃B可能互为同分异构体
c.当m=12时,烃A一定为烷烃
d.当n=11时,烃B可能的分子式有2种
(2)若烃A为链烃,且分子中所有碳原子都在同一条直线上,则A的结构简式为 。
(3)若烃A为链烃,且分子中所有碳原子一定共面,在一定条件下,1mol A最多可与1mol H2加成,则A的名称是 。
(4)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量的浓硫酸,浓硫酸的质量增加1.26g,再通过足量的碱石灰,碱石灰的质量增加4.4g,则烃B的分子式为 ;若其苯环上的一溴代物只有一种,则符合此条件的烃B有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某元素原子共有3个价电子,其中一个价电子位于第三能层![]() 能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
(2)![]() 、
、![]() 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出![]() 原子的核外电子排布式:______。
原子的核外电子排布式:______。
电离能/ |
|
|
|
|
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽油不仅是最重要的燃料,而且是重要的化工原料,它既可以裂解得到气态化工原料如乙烯等,还可以在催化剂催化下改变分子结构,由链烃变成芳香烃,如己烷变成苯,庚烷变成甲苯等。又知丙烯的化学性质和乙烯相似,请根据如图,回答有关问题:
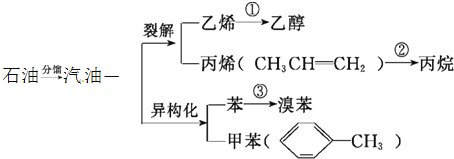
(1)写出相应的化学方程式:
![]() ______;
______;
![]() ______;
______;
![]() ______;
______;
(2)甲苯分子里苯环上一个氢原子被硝基取代后的产物有 ______ 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com