
| A、c(CH3COO-)>c(H+)>c(Na+ )>c(OH-) |
| B、c(Na+ )>c(OH-)>c(CH3COO-)>c(H+ ) |
| C、c(OH-)>c(Na+ )>c(H+ )>c(CH3COO-) |
| D、c(Na+ )>c(CH3COO-)>c(OH-)>c(H+ ) |


科目:高中化学 来源: 题型:
| A、①②④⑥ | B、①②⑤⑥ |
| C、①②③⑥ | D、都正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当0.10mol?L-1醋酸溶液pH=3.0时达到电离平衡状态 |
| B、0.10mol?L-1醋酸溶液和0.0010mol?L-1醋酸溶液的c(H+)之比为100:1 |
| C、0.10mol?L-1醋酸钠溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、0.1 mol/L NaHCO3溶液:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
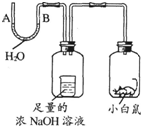
| A、A处上升,B处下降 |
| B、A、B两处都下降 |
| C、A处下降,B处上升 |
| D、A、B两处都不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| B、溶液中导电能力的强弱主要与溶液中的离子浓度大小和离子所带电荷数有关 |
| C、强弱电解质的本质区别是溶液导电能力的强弱 |
| D、强电解质的溶液中只有离子,没有分子存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 |
| B、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| C、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
| D、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
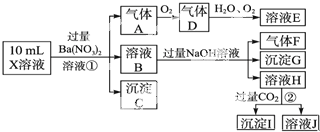
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com