
【题目】下列事实的解释合理且表达正确的是( )
A.NH4Cl溶液呈酸性:NH4++2H2O![]() NH3·H2O+H3O+
NH3·H2O+H3O+
B.氨气溶于水,溶液呈碱性:NH3·H2O=NH4++OH-
C.NaHSO4溶液可以导电:NaHSO4![]() Na++H++SO42-
Na++H++SO42-
D.常温下,饱和H2CO3溶液pH=4:H2CO3![]() 2H++CO32-
2H++CO32-
 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是( )
A.铁触媒有利于合成氨反应
B.夏天开启啤酒瓶盖后,瓶中立刻泛起大量泡沫
C.对装有N2O4和NO2混合气体的密闭烧瓶加热,颜色变深
D.合成氨反应:![]()
![]()
![]() ,为使氨的产率提高,理论上应采取低温高压的措施
,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有室温下四种溶液,有关叙述不正确的是( )
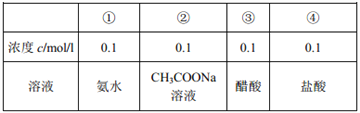
A. 
20 mL (1)溶液中逐滴加入(3)溶液,溶液导电能力变化如图
B. (2)、(3)两溶液等体积混合,离子浓度: 2c(Na+)= c(CH3COO-)+ c(CH3COOH)
C. (1)、(4)两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+) >c(OH-)
D. 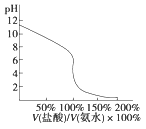
用(4)滴定(1),滴定曲线如图,可用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H-H键的键能为436kJ· mol-1,H-N键的键能为391 kJ· mol-1,根据热化学方程式:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
A.431 kJ· mol-1B.649 kJ· mol-1C.945.6 kJ· mol-1D.896 kJ· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷燃烧可以通过以下两种途径:
途径Ⅰ:C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-a kJ·mol-1
途径Ⅱ:C3H8(g)―→C3H6(g)+H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+9O2(g)===6CO2(g)+6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH=-d kJ·mol-1 (a、b、c、d均为正值)
请回答下列问题:
(1)由于C3H8(g)→C3H6(g)+H2(g)的反应中,反应物具有的总能量________(填“大于”、“小于”或“等于”)生成物具有的总能量,那么在化学反应中,反应物就需要________(填“放出”或“吸收”)能量才能转化为生成物,因此其反应条件是__________。
(2)按途径Ⅱ反应,1 mol C3H8完全燃烧时放出的热量为________ kJ(用含b、c、d的代数式表示),等量的丙烷通过两种途径完全燃烧时,途径Ⅰ放出的热量________(填“大于”、“小于”或“等于”)途径Ⅱ放出的热量。
(3)a与b、c、d的数学关系式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次氯酸可用于杀菌消毒,已知![]() 时:①
时:①![]() 、②
、②![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.在![]() 时,次氯酸的电离方程式及热效应可表示为:
时,次氯酸的电离方程式及热效应可表示为:![]()
B.将![]() 与
与![]() 混合后的溶液,一定存在:
混合后的溶液,一定存在:![]()
C.将![]() 与
与![]() 等体积混合后的溶液,溶液显碱性,则存在:
等体积混合后的溶液,溶液显碱性,则存在:![]()
D.已知酸性![]() ,则等浓度
,则等浓度![]() 和NaClO的混合液中:
和NaClO的混合液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨为重要化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+216.4KJ/mol
CO(g)+3H2(g) △H=+216.4KJ/mol
b.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
则反应CH4(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=______。
CO2(g)+4H2(g) △H=______。
(2)起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度关系如图。
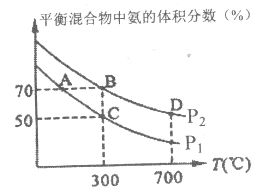
①恒压时,反应一定达到平衡状态的标志是______(填序号):
A.N2和H2的转化率相等 B.反应体系密度保持不变
C.![]() 的比值为3:2 D.
的比值为3:2 D.![]() =2
=2
②P1______P2(填“>”、“<”、“=”,下同):反应平衡常数:B点______D点;
③C点H2的转化率______;(数值保留0.1%)在A、B两点条件下,该反应从开始到平衡时生成氢气平均速率:v(A)______v(B)(填“>”、“<”、“=”)。
(3)已知25℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为______________(已知25℃时,H2SO3的电离平衡常数Ka1=1×10-2,Ka2=1×10-7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是
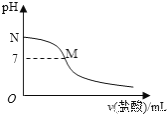
A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
科目:高中化学 来源: 题型:
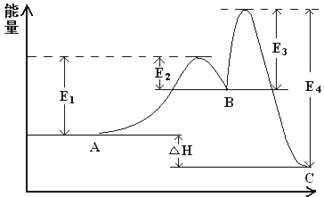
【题目】某反应由两步反应A![]() B
B![]() C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)。下列有关叙述正确的是( )
C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)。下列有关叙述正确的是( )
![]()
A. 两步反应均为吸热反应 B. 三种化合物的稳定性顺序:B﹤A﹤C
C. 加入催化剂不改变反应的焓变,但能提高转化率 D. 整个反应的ΔH=E1-E2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com