
【题目】关于 2NaOH(s)+H2SO4(aq)→Na2SO4(aq)+2H2O(l)+Q kJ 说法正确的是( )
A.NaOH(s)溶于水的过程中扩散吸收的能量大于水合释放的能量
B.Q<0
C.NaOH(s)+1/2H2SO4(aq)→1/2Na2SO4(aq)+H2O(l)+1/2QkJ
D.若将上述反应中的NaOH(s)换成NaOH(aq),则Q′>Q
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂,热分解产生锰酸钾、二氧化锰、氧气。完成下列填空:
I. 已知:①MnO2(s)=Mn(s)+O2(g) ΔH=+520kJ/mol
②S(s)+O2(g)=SO2(g) ΔH=-297kJ/mol
③Mn(s)+2O2(g)+S(s)=MnSO4(s) ΔH=-1065kJ/mol
(1)固体MnO2和二氧化硫气体反应生成MnSO4固体的热化学方程式为________________。
II.草酸钠滴定法测定高锰酸钾的质量分数涉及到的反应:
C2O42-+2H+→H2C2O4(草酸)
5H2C2O4+2MnO4-+6H+→2Mn2++10CO2↑+8H2O
(2)上述反应在75~80℃进行比较合适,当加热温度大于90℃时,会导致草酸钠消耗增多,其原因是______________________。
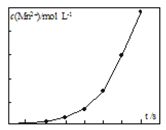
(3)将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应溶液中Mn2+的浓度随反应时间t的变化如图,Mn2+浓度变化由缓慢增大后迅速增大的原因是____________________________。
III .KMnO4是一种常用消毒剂。
(4)KMnO4消毒机理与下列物质相似的是__________(填序号)。
A. 双氧水 B.消毒酒精(75%) C.肥皂水 D. 84消毒液(NaClO溶液)
(5)KMnO4消毒效率(用单位质量转移的电子数表示)是NaClO的______倍(保留两位小数)。
(6)测定KMnO4产品的纯度可用标准Na2SO3溶液滴定。
①配制250ml0.1000mol/L标准Na2SO3溶液,需要使用的玻璃仪器有烧杯、胶头滴管、量筒、玻璃棒和____________。
②取某KMnO4产品0.7000g溶于水,并加入____________进行酸化。
A. 稀盐酸 B.稀硫酸 C.硝酸 D. 次氯酸
③将②所得溶液用0.1000mol/L标准Na2SO3溶液进行滴定,滴定至终点记录实验消耗Na2SO3溶液的体积。重复步骤②、③,三次平行实验数据如表:
实验次数 | 1 | 2 | 3 |
消耗Na2SO3溶液体积/ml | 19.30 | 20.98 | 21.02 |
(有关离子方程式为:2MnO4- + 5SO32- + 6H+ =5SO42- + 2Mn2+ + 3H2O)
计算该KMnO4产品的纯度为__________。(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)AgNO3的水溶液呈________(填“酸”、“中”、“碱”)性,实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以____(填“促进”、“抑制”)其水解。
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρ g/cm3,Xm+的浓度为c mol/L,则该难溶物XnYm的溶度积常数为Ksp=________。
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈_____(填“酸”、“中”、“碱”)性,混合时醋酸体积________(填“大于”、“等于”或“小于”)氢氧化钠溶液体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是
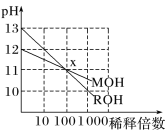
A. MOH是一种弱碱
B. 在x点,c(M+)=c(R+)
C. 稀释前,c(ROH)=10c(MOH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2、NH4HSO4用途广泛。请回答下列问题:
(1)常温时,0.1 mol·L-1 NH4Al(SO4)2溶液的pH=3。则溶液中c(NH4+)+c(NH3·H2O)_______c (Al3+) + c[Al(OH)3](填“﹥”、“﹤”或“=”);2c(SO42-)- c(NH4+)-3c(Al3+)=________mol·L-1(填数值)。
(2)80℃时,0.1 mol·L-1 NH4Al(SO4)2溶液的pH小于3,分析导致pH随温度变化的原因是________________________ (用离子方程式并结合文字叙述回答)。
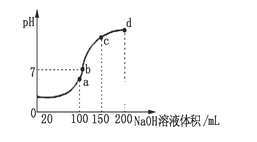
(3)常温时,向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加 0.1 mol·L-1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示。向NH4HSO4溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为__________________。
(4)常温时,浓度为0.1 mol·L-1Na HSO4溶液与pH=12的氢氧化钠溶液反应后混合液pH=2则二者体积比为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了研究氯气的性质,做以下探究实验。向KI溶液通入氯气溶液变为黄色;继续通入氯气一段时间后,溶液黄色退去,变为无色;继续通入氯气,最后溶液变为浅黄绿色,查阅资料:I2+I-I3-,I2、I3-在水中均呈黄色。
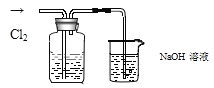
(1)为确定黄色溶液的成分,进行了以下实验:取 2~3 mL 黄色溶液,加入足量 CCl4,振荡静置,CCl4层呈紫红色,说明溶液中存在______,生成该物质的化学方程式为______,水层显浅黄色,说明水层显黄色的原因是______;
(2)继续通入氯气,溶液黄色退去的可能的原因______;
(3)NaOH 溶液的作用______,反应结束后,发现烧杯中溶液呈浅黄绿色,经测定该溶液的碱性较强,一段时间后溶液颜色逐渐退去,其中可能的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向1L密闭容器中加入2 mol N2和7molH2,发生反应N2+3H2![]() 2NH3,2分钟末时,测得剩余氮气为1mol,下列有关该反应的反应速率的描述中不正确的是()。
2NH3,2分钟末时,测得剩余氮气为1mol,下列有关该反应的反应速率的描述中不正确的是()。
A.υ(N2)= 0.5 mol/(L·min)B.υ(H2)= 1.5 mol/(L·min)
C.υ(NH3)= 1 mol/(L·min)D.υ(N2)=1mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W在大气中有两种同素异形体且均能支持燃烧,X的原子半径是所有短周期主族元素中最大的,非金属元素Y的原子序数是Z的最外层电子数的2倍。下列叙述不正确的是( )
A.Y、Z的氢化物稳定性Y>Z
B.Y单质的熔点高于X单质
C.X、W、Z能形成具有强氧化性的XZW
D.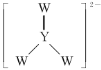 中W和Y都满足8电子稳定结构
中W和Y都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:可逆反应Cu(s)+CO2(g) CuO(s)+CO(g) △H>0
(1)能判断该反应达到平衡的依据是__________。
A.容器内压强保持不变 B.c(CO)保持不变
C.υ正(CO2)=υ逆(CO) D.c(CO2)=c(CO)
(2)该反应的平衡常数表达式为_________________ ;若该反应在体积固定的密闭容器中进行,反应物为过量Cu(s)和CO2,在一定条件下达到平衡状态,如果改变下列条件再达平衡
Ⅰ.升高温度,CO的平衡浓度__________(选填“增大”、“减小”、“不变”下同)
Ⅱ.再通入CO2,CO2的平衡转化率___________
(3)该反应的逆反应速率随时间变化情况如图:从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是_______________

a.升温 b.增大CO2的浓度 c.使用催化剂 d.增压
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com