
| A. | 96g | B. | 74g | C. | 82.5g | D. | 无法计算 |
分析 因为原来的40g固体是Mg,Zn,Fe单质的总质量,136g蒸干所得固体是MgSO4、FeSO4、ZnSO4的总质量,那么136g-40g=96g就是加进来的硫酸根的质量,因为硫酸根的分子量是96,所以加入的硫酸根是1mol,加入一定量的氢氧化钠溶液使金属离子全部转化为沉淀,因为1mol的硫酸根离子带2mol的负电荷,所以根据电荷守恒,金属离子结合氢氧根离子的物质的量为2mol,由此分析解答.
解答 解:因为原来的40g固体是Mg,Zn,Fe单质的总质量,136g蒸干所得固体是MgSO4、FeSO4、ZnSO4的总质量,那么136g-40g=96g就是加进来的硫酸根的质量,因为硫酸根的分子量是96,所以加入的硫酸根是1mol,加入一定量的氢氧化钠溶液使金属离子全部转化为沉淀,因为1mol的硫酸根离子带2mol的负电荷,所以根据电荷守恒,金属离子结合氢氧根离子的物质的量为2mol,所以沉淀的质量是40+2×17=74g,
故选B.
点评 本题考查混合物的计算、氧化还原反应的计算,题目难度中等,明确电子转移的数目和氢氧根离子之间的关系,为解答该题的关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
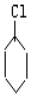 $→_{②}^{NaOH、乙醇}$
$→_{②}^{NaOH、乙醇}$ $→_{③}^{溴的CCl_{4}溶液}$B$\stackrel{④}{→}$
$→_{③}^{溴的CCl_{4}溶液}$B$\stackrel{④}{→}$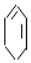

 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 60gSiO2中含Si-O键的个数为2NA | |
| C. | 12 g石墨中含有C-C键的个数为1.5NA | |
| D. | 36 g戊烷中共价键的个数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中的甲苯(溴水) | B. | 溴苯中的溴(苯) | ||
| C. | 乙烷中的乙烯(酸性高锰酸钾) | D. | 95.6%乙醇中的水(生石灰) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 原子结构或性质 |
| A | 其形成的一种同位素元素在考古中可推测化石的年代 |
| B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
| C | 地壳中含量最多的元素 |
| D | D原子的最外层电子数与其电子层数相同,是地壳中含量最多的金属元素 |
| E | 其单质主要存在于火山口附近 |
| F | 生活中常见的金属,它的某种氧化物均有磁性 |
| G | G原子与D原子同周期,且原子半径是同周期元素中最大的 |
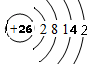 ;
; ,
,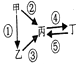
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 检验FeCl3溶液的Fe2+ | 向溶液中加入酸性KMnO4溶液 |
| B | 比较CH3COOH和HCN的酸性强弱 | 用pH计分别测定CH3COONa、NaCN饱和溶液的pH |
| C | 制备H2SiO3胶体 | 向Na2SiO3溶液中滴加过量HCl |
| D | 除去乙酸乙酯中的CH3COOH | 加入饱和Na2CO3溶液,振荡后静置,分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{14}$ mol•L-1 | B. | $\frac{4}{5}$ mol•L-1 | C. | $\frac{1}{28}$ mol•L-1 | D. | $\frac{1}{42}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
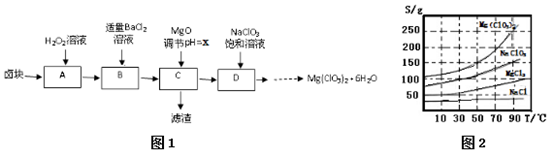
| 化学式 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.8x10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com