
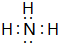 .
. 分析 根据元素周期律的递变规律比较元素、单质以及对应化合物的性质,结合原子结构解答电子数为10的化合物,氮元素的气态氢化物的水溶液显碱性,则对应氢化物为氨气,氨气中存在3个氮氢键,氮原子最外层8个电子,据此书写电子式.
解答 解:(1)在原子序数1-18号元素中,与水反应最剧烈的金属是Na,金属性最强,
故答案为:Na;
(2)与水反应最剧烈的非金属单质是F2,F元素的非金属性最强,
故答案为:F2;
(3)原子半径最小的元素是H,原子核外只有1个电子,
故答案为:H;
(4)最稳定气态氢化物对应的元素的非金属性应最强,为HF,
故答案为:HF;
(5)最高价氧化物对应水化物的酸性最强的元素为Cl,非金属性仅次于F、O,但F、O无正价,不存在对应的酸,化学式是HClO4,
故答案为:HClO4;
(6)因H的质子数为1,C的质子数为6,N的质子数为7,O的质子数为8,F的质子数为9,Ne的质子数为10,在中性微粒中,质子数等于电子数,
则CH4、NH3、H2O、HF、Ne的电子数都是10,
故答案为:CH4、NH3、H2O、HF、Ne;
(7)氮元素的气态氢化物的水溶液显碱性,则对应氢化物为氨气,分子中H原子与N原子之间形成1对共用电子对,电子式为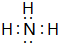 ,
,
故答案为: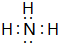 .
.
点评 本题考查原子结构和元素周期律的关系,题目难度不大,注意基础知识的积累.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:解答题
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 1.5mol | C. | 2mol | D. | 2.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
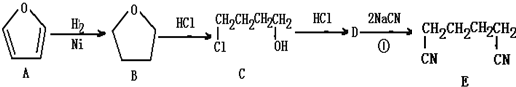
| A. | A→B的反应属于加成反应 | B. | B→C的反应属于酯化反应 | ||
| C. | C→D的反应属于消去反应 | D. | D→E的反应属于加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将乙醛滴入银氨溶液中,加热煮沸制银镜 | |
| B. | 苯与溴水反应制取溴苯 | |
| C. | 向少量苯酚稀溶液中逐滴加入饱和溴水,边加边振荡,观察沉淀 | |
| D. | 1mol•L-1CuSO4溶液2mL和0.5mol•L-1NaOH溶液4mL混合后加入40%的乙醛溶液0.5mL,加热煮沸观察沉淀的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
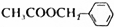 )是其中的一种,它可以从茉莉花香中提取,也可以用甲苯和乙醇为原料进行人工合成,一种合成路线如下:
)是其中的一种,它可以从茉莉花香中提取,也可以用甲苯和乙醇为原料进行人工合成,一种合成路线如下:
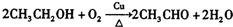 .
. ,名称为苯甲醇.
,名称为苯甲醇.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳极发生还原反应,其电极反应式:Ni2++2e-═Ni | |
| B. | 电解过程中,阳极质量的减少与阴极质量的增加相等 | |
| C. | 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ | |
| D. | 电解后,可以从电解槽底部的阳极泥中回收Cu和Pt |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
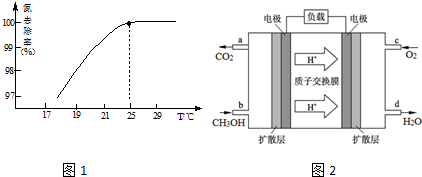
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com