
| ���� | SiCl4 | SiHCl3 | FeCl3 | AlCl3 |
| �۵�/�� | -70 | -128.2 | 306 | -- |
| �е�/�� | 57.6 | 31.85 | 315 | 181 ���� |
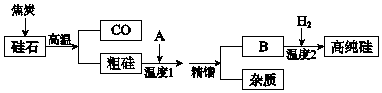
���� ���ʯ��SiO2��99.0%������������Al2O3��Fe2O3�ȣ��мӽ�̿����Ҫ������ӦSiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����ͬʱ��̿��Al2O3��Fe2O3��ԭΪ��������������ֹ�ͨA����õ�SiCl4��FeCl3��AlCl3���ٿ����¶Ⱦ���õ�B��SiCl4����A��HCl��B��SiHCl3��ͨ�������õ��ߴ��裬�ݴ˷������
��� �⣺��1���ӹ�ʯ�еõ��ֹ�Ļ�ѧ����ʽ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����ͬʱ��̿��Al2O3��Fe2O3��ԭΪ������������
�ʴ�Ϊ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO��������
��2����ӦSiO2+3C$\frac{\underline{\;����\;}}{\;}$SiC+2CO����C�Ļ��ϼ������ߵ�������̼��Ҳ�н��͵�SiC��˵��C����������Ҳ����ԭ����
�ʴ�Ϊ��̼��
��3����A��������B�����Ȼ��裬����õ�����SiCl4���ӱ������ݿ�֪�������¶�55��60��ʱ��SiCl4�� FeCl3��AlCl3���룻
�ʴ�Ϊ��a��FeCl3��AlCl3��
��4����A��HCl��B��SiHCl3����B��ͨ����������ӦSiHCl3+H2$\frac{\underline{\;�¶�2\;}}{\;}$Si+3HCl��HCl��ѭ�����ã��ʴ�Ϊ��HCl��
���� ���⿼����ѧ�����ۺϷ���������Ҫ��ѧ���߱��й����ʵĻ���֪ʶ���н��ʵ���������������Ŀ�Ѷ��еȣ�


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȫ��ͨ����ֽ | B�� | �ж����ЧӦ | ||
| C�� | ���ײ�����ͨ����Ĥ | D�� | �е�Ӿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al��OH��3�ֽ� | B�� | CO2+OH- | C�� | Al+OH-+H2O | D�� | Al2O3+OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������� | �¶�/�� | ��ʼ���ʵ���/mol | ƽ�����ʵ���/mol | ||
| H2 | SO2 | H2 | SO2 | ||
| ������ | 300 | 0.3 | 0.1 | / | 0.02 |
| ������ | 300 | 0.6 | 0.2 | / | / |
| ������ | 240 | 0.3 | 0.1 | / | 0.01 |
| A�� | �÷�Ӧ������Ӧ���� | |
| B�� | ����ƽ��ʱ����������SO2��ת���ʱ�������Ĵ� | |
| C�� | 240��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ1.08��104 | |
| D�� | ����ƽ��ʱ���������е�����Ӧ���ʱ��������еĴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | � | NaNO3 |
| B | ��ʯ�� | 2CaSO4•H2O |
| C | ���� | KAl��SO4��2 |
| D | �̷� | FeCl2•7H2O |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1��1 | B�� | 1��2��3 | C�� | 3��1��1 | D�� | 6��3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڻ�Ϊˮ�Ĺ��̡�H��0����S��0 | |
| B�� | ����������������������£�ʹ�ô��������Ըı仯ѧ��Ӧ���еķ��� | |
| C�� | �ڳ����£����ȷ�Ӧһ�����Է����У����ȷ�Ӧ�������Է����� | |
| D�� | NH4HCO3��s��?NH3��g��+H2O��g��+CO2��g����H=+185.57kJ/mol�����Է����У�ԭ������ϵ���Է�������Ҷ����ӵķ���ת������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ڷ�Ӧ��H2��g��+Cl2��g��=2HCl ��g����H=-a kJ/mol�������ƻ��ɻ�ѧ�����յ��������γ��»�ѧ���ͷŵ������� | |
| B�� | 2MnO��s��+O2��g���T2MnO2��s�����÷�Ӧ�ڵ��������Է����У������H��0 | |
| C�� | �ø����pH��ֽ���ij��ˮ��pH=3.1 | |
| D�� | �����ڴ��е��ִ�ˮ���ϵIJ��ֱ�ˮ���µIJ��ָ�ʴ��������Ϊˮ�������绯ѧ��ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | С�մ������θ�ᷴӦ������С�մ�����θ����� | |
| B�� | �ý��ݹ����������Һ�Ĺ���������ˮ�������˼ӳɷ�Ӧ | |
| C�� | ʳƷ�������������ۡ��Ȼ��ơ�̿�۵ȣ�������ԭ���������������ʴ��ͬ | |
| D�� | ������������������Һ���ȣ�������ع��ͣ��ӹ����IJ��������ͣ�������ͣ����͡�ú�͡����͵ȣ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com