

| A. | 当m2-m3=2.96 g时,Fe3O4的质量至少为2.32g | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 要确定混合物中是否含有Al,可取A加入适量稀盐酸 | |
| D. | 当m1>m2时,溶液a中的阴离子只有1种 |
分析 A.引固体质量改变的金属氧化物的溶解,和三价铁与铜单质之间的氧化还原反应;
B.Fe3O4与盐酸反应生成氯化铁和氯化亚铁,三价铁离子有强氧化性;
C.金属氧化物与酸反应生成水,无氢气,而铜与盐酸不反应;
D.当m1>m2时,说明至少有Al2O3、Al两者中的一种,且生成了偏铝酸钠溶液.
解答 解:A.根据反应方程式Fe3O4+8H+=Fe2++2Fe3++4H2O、Cu+2Fe3+=Cu2++2Fe2+可知若Fe3O4产生的Fe3+恰好与Cu反应,二者的物质的量关系是:Fe3O4~2Fe3+~Cu,即232g的Fe3O4反应会消耗64g Cu,固体总质量减轻:232g+64g=296g,所以当m2-m3=2.96g时,Fe3O4的反应消耗质量为2.32 g,若Fe3O4过量则其质量大于2.32 g,因此Fe3O4至少为2.32 g,故A正确;
B.Fe3O4与盐酸反应生成氯化铁和氯化亚铁,三价铁离子有强氧化性,发生反应为:Cu+2Fe3+═Cu2++2Fe2+,故B正确;
C.金属氧化物与酸反应生成水,无氢气,而铜与盐酸不反应,可取A加入适量稀HCl,如果有气体产生,证明铝的存在,故C正确;
D.铝、氧化铝都能和氢氧化钠反应,Fe3O4、Cu和氢氧化钠不反应,当m1>m2时,说明至少有Al2O3、Al两者中的一种,且生成了偏铝酸钠溶液,而过量的氢氧化钠,阴离子大于一种,故D错误;
故选D.
点评 本题考查常见金属元素及化合物的综合应用,题目难度中等,要通过实验现象得出结论,再结合定量计算得出结论,明确发生反应的实质为解答关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:多选题
| A. | 与足量的澄清石灰水反应的现象不同 | |
| B. | 通入BaCl 2溶液时现象相同 | |
| C. | 通入Ba(NO3)₂溶液时现象相同 | |
| D. | 通入石蕊溶液时现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.
甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
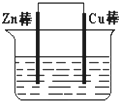 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性NaHCO3<Na2CO3 | B. | 常温时水中溶解度NaHCO3>Na2CO3: | ||
| C. | 与盐酸反应的速率:NaHCO3>Na2CO3 | D. | 相对分子质量:NaHCO3<Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 色态 | 溶于碱 | 常温常压 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃ 红黄色液体 | 生成亚氯酸盐和氯酸盐 | 不稳定 | 爆炸 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温、高压 | B. | 适宜的温度、高压、催化剂 | ||
| C. | 低温、低压 | D. | 高温、高压、催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| B. | 12g石墨和C60的混合物中质子总数一定为6 NA个 | |
| C. | 25℃时,1L0.1mol•L-1FeCl3溶液中含有0.1 NA 个Fe(OH)3胶体粒子 | |
| D. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
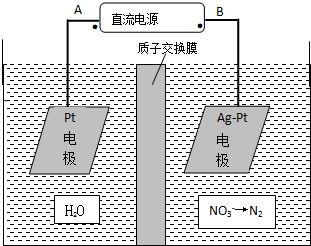 硝酸是一种重要的化工原料,工业上一般以氨气为原料来制备硝酸.请回答:
硝酸是一种重要的化工原料,工业上一般以氨气为原料来制备硝酸.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com