
 ;
; ;
; ;
; (填结构简式).
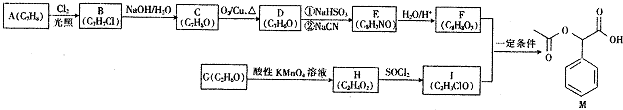
(填结构简式). 分析 根据流程图,A中应该含有苯环,A为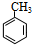 ,在光照时侧链与氯气发生取代反应,B为
,在光照时侧链与氯气发生取代反应,B为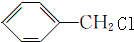 ;B在氢氧化钠溶液中水解生成C,则C为
;B在氢氧化钠溶液中水解生成C,则C为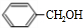 ,C氧化生成D为
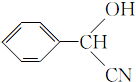
,C氧化生成D为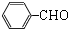 ;根据已知信息,E为
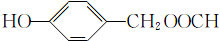
;根据已知信息,E为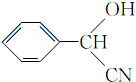 ,F为
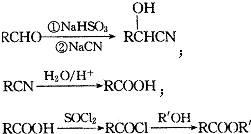
,F为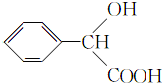 ,G为乙醇(CH3CH2OH),H为乙酸(CH3COOH),根据信息知,I为CH3COCl,F和I在一定条件下 反应生成M(
,G为乙醇(CH3CH2OH),H为乙酸(CH3COOH),根据信息知,I为CH3COCl,F和I在一定条件下 反应生成M(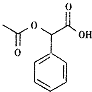 ).
).
解答 解:根据流程图,A中应该含有苯环,A为 ,在光照时侧链与氯气发生取代反应,B为
,在光照时侧链与氯气发生取代反应,B为 ;B在氢氧化钠溶液中水解生成C,则C为
;B在氢氧化钠溶液中水解生成C,则C为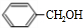 ,C氧化生成D为
,C氧化生成D为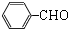 ;根据已知信息,E为
;根据已知信息,E为 ,F为
,F为 ,G为乙醇(CH3CH2OH),H为乙酸(CH3COOH),根据信息知,I为CH3COCl,F和I在一定条件下 反应生成M(
,G为乙醇(CH3CH2OH),H为乙酸(CH3COOH),根据信息知,I为CH3COCl,F和I在一定条件下 反应生成M( ).
).
(1)根据上述分析,A为甲苯,F为 ,所含官能团是羟基和羧基,
,所含官能团是羟基和羧基,
故答案为:甲苯;羟基、羧基;
(2)C为苯甲醇,C氧化生成D(苯甲醛);H为乙酸(CH3COOH),根据信息知,H与二氯亚砜发生取代反应生成I(CH3COCl),
故答案为:氧化反应;取代反应;
(3)根据上述分析,E为 ,故答案为:
,故答案为: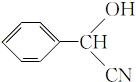 ;
;
(4)根据信息,F和I在一定条件下发生取代反应生成M,反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(5)F为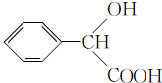 ,其同分异构体满足:①能与FeCl3溶液发生显色反应,表明分子结构中存在酚羟基;②能发生水解反应,表明分子结构中含有酯基;③苯环上只有两个取代基,符合上述条件的F的同分异构体的结构简式有:
,其同分异构体满足:①能与FeCl3溶液发生显色反应,表明分子结构中存在酚羟基;②能发生水解反应,表明分子结构中含有酯基;③苯环上只有两个取代基,符合上述条件的F的同分异构体的结构简式有: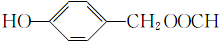 (包括邻位、间位和对位3种);
(包括邻位、间位和对位3种);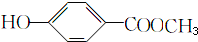 (包括邻位、间位和对位3种);
(包括邻位、间位和对位3种);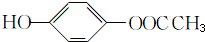 (包括邻位、间位和对位3种),共9种,其中核磁共振氢谱显示有5组峰,且峰面积之比为1:1:2:2:2的是
(包括邻位、间位和对位3种),共9种,其中核磁共振氢谱显示有5组峰,且峰面积之比为1:1:2:2:2的是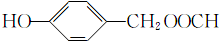 ,
,
故答案为:9; .
.
点评 本题考查了有机合成与推断,充分利用有机物分子式、反应条件及给予的信息进行分析,熟练掌握官能团的性质与转化,较好的考查学生信息获取与知识迁移运用.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
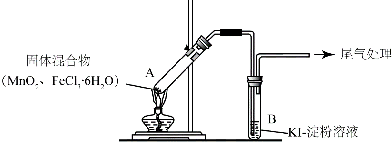
| 操作 | 现象 |
| 点燃酒精灯,加热 | iA中部分固体溶解,上方出现白雾 ii稍后,产生黄色气体,管壁附着黄色液滴 iiiB中溶液变蓝 |
| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈浅橙色;未检出Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60% | B. | 77.8% | C. | 48.0% | D. | 34.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
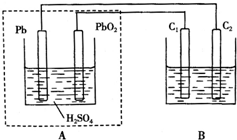 用铅蓄电池作电源电解某溶液100mL.已知该溶液中含SO2、KI,其物质的量浓度均为0.1mol/L,如图所示(C1、C2为石墨电极),下列说法正确的是( )
用铅蓄电池作电源电解某溶液100mL.已知该溶液中含SO2、KI,其物质的量浓度均为0.1mol/L,如图所示(C1、C2为石墨电极),下列说法正确的是( )| A. | 铅蓄电池工作一段时间后A溶液的pH变小 | |
| B. | 当B烧杯中I-的浓度降为0.05mol/L时,消耗A中的H2SO4的物质的量为0.025mol | |
| C. | 当C1、C2两极均产生气体时,应有至少3.6×1022个电子从电路中流过 | |
| D. | 铅蓄电池工作时负极电极反应式为:PbO2-2e-+H2SO4═PbSO4+2H2O+SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应速率等于逆反应速率 | B. | 反应物和生成物浓度不再发生变化 | ||
| C. | 反应体系中混合物的组成保持不变 | D. | 正、逆反应速率都为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
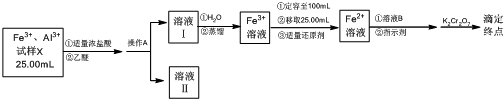
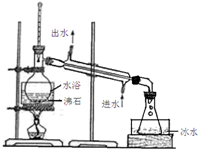
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
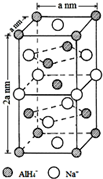 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.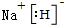 .
. (标明配位键).
(标明配位键).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com