
分析 (1)水为弱电解质,能够电解出氢离子和氢氧根离子,在溶液中存在电离平衡;加入酸溶液和碱溶液能够抑制水的电离,加入能够水解的盐促进了水的电离,据此进行判断;
(2)根据酸的强弱、碱的强弱以及盐类的水解的酸碱性比较;
(3)将②和③等体积混合后,②醋酸③氢氧化钠反应后得到醋酸钠溶液,醋酸根离子水解溶液显碱性;
(4)25℃时,将pH=13的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=12,说明氢氧根离子过量,计算剩余氢氧根离子浓度计算得到溶液体积比;
(5)将a mol/L的氨水溶液与0.1mol/L①硫酸溶液等体积混合后,溶液呈中性,c(OH-)=c(H+)=10-7mol/L,结合溶液中电荷守恒得到,c(NH4+)+c(H+)=c(OH-)+2c(SO42-),得到c(NH4+)=2c(SO42-),氨水平衡常数K=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$;
解答 解:(1)①硫酸是酸抑制水的电离,②醋酸是酸抑制水的电离,③氢氧化钠是碱抑制水的电离,④氯化铵溶液中铵根离子水解促进水的电离,
故答案为:④;
(2)等浓度的溶液中,显酸性的①硫酸②醋酸④氯化铵,其中氯化铵是水解显示的酸性,硫酸是二元酸,醋酸是一元弱酸,显碱性的为③氢氧化钠,则)①②③④四种溶液中pH由大到小的顺序是③>④>②>①,
故答案为:③>④>②>①
(3)醋酸③氢氧化钠等体积混合后,反应得到醋酸钠溶液,醋酸根离子水解溶液显碱性,溶液离子浓度大小为:(Na+)>c(CH3COO-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
(4)25℃时,将pH=13的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=12,剩余氢氧根离子浓度c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$=0.01mol/L,pH=13的NaOH溶液aL中氢氧根离子浓度为$\frac{1{0}^{-14}}{1{0}^{-13}}$=0.1mol/L,与pH=2的H2SO4溶液bL中氢离子浓度为0.01mol/L,
$\frac{0.1mol/L×aL-0.01mol/L×bL}{aL+bL}$=0.01mol/L
则a:b=9:1,
故答案为:9:1;
(5)将a mol/L的氨水溶液与0.1mol/L①硫酸溶液等体积混合后,溶液呈中性,c(OH-)=c(H+)=10-7mol/L,结合溶液中电荷守恒得到,c(NH4+)+c(H+)=c(OH-)+2c(SO42-),得到c(NH4+)=2c(SO42-),氨水平衡常数K=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{2×0.05mol/L×1{0}^{-7}mol/L}{\frac{a}{2}mol/L-2×0.05mol/L}$=$\frac{2×1{0}^{-8}}{a-0.2}$
故答案为:$\frac{2×1{0}^{-8}}{a-0.2}$;
点评 本题考查了溶液离子浓度大小的比较以及盐类的水解和弱电解质的电离等问题、水的电离及其影响因素、溶液PH计算,题目难度中等,注意掌握水的电离及影响,明确酸碱溶液抑制水的电离,含有弱酸根或者弱碱根离子的盐能够促进水的电离、影响盐类水解以及电解质的电离的因素.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L氯气与足量的铜充分反应 | B. | 0.2mol浓硫酸与足量铜反应 | ||
| C. | 46g金属钠与足量的水反应 | D. | 56g铁与足量稀硝酸溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酒精在氧气中燃烧 | B. | 在硫酸中加入铝粉 | ||
| C. | 将二氧化碳气体通入烧碱中 | D. | 向盐酸中加入铁钉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
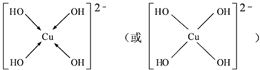 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将实验完剩余的金属钠放回原试剂瓶中 | |
| B. | 测定熔融氢氧化钠的导电性,可在铁质坩埚中熔化氢氧化钠固体后进行测量 | |
| C. | 制备Fe(OH)3胶体通常是将饱和氯化铁溶液煮沸,直至呈红褐色时停止加热 | |
| D. | 在饱和NaOH溶液中加一定量Na2O2,充分反应后恢复到原温度,有晶体析出,溶液质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘是人体必需微量元素,所以应多吃富含高碘酸的食物 | |
| B. | “血液透析”运用了胶体的性质 | |
| C. | 过氧化钠可作为高空飞行或潜水装置中的供氧剂 | |
| D. | 大力开发太阳能、风能、水能等新能源,减少煤、石油等化石燃料的使用,有利于实现“低碳经济” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2014年西非国家爆发埃博拉病毒,双氧水、高锰酸钾溶液可以完全灭活该病毒感染性,其消毒原理和漂白粉消毒饮用水相同 | |
| B. | 2015年初公益调查《柴静雾霾调查:穹顶之下》发布,引起社会强烈反响.雾霾中PM2.5属于胶体 | |
| C. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| D. | 汽油、煤油、植物油都是油,但它们的主要成分不相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com