
【题目】用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:
4HCl(g) + O2(g)![]() 2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
A. 氯化氢的转化率不再改变 B. 气体的质量不再改变
C. 断开4 mol H-Cl键的同时生成4 mol H-O键 D. n(HCl)∶n(O2)∶n(Cl2)∶n(H2O)=4∶1∶2∶2
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】乙醇是一种常用的工业燃料,燃料乙醇的生产过程可由下图表示:
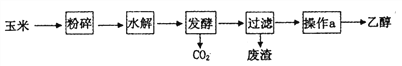
(1)粉碎玉米的目的是____________。
(2)生产过程中检验玉米中是否完全水解的方法是_________。
(3)请写出“发酵”过程中反应的化学方程式_____________;发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途:______________________、________________________
(4)操作a的名称是_________,检验乙醇中是否含有水可以用试剂______。
(5)根据上述生产过程,用5吨含淀粉70%的玉米,假设淀粉水解的百分率为85%,发酵过程的转化率为60%,则最终可以制得无水乙醇________kg(小数点后保留一位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体。请回答下列问题(用元素符号或化学式表示):
(1)X元素位于周期表的________区。
(2)基态D原子的价电子轨道表示式是______,其第一电离能反常地低于同周期前一种元素,原因是_______。
(3)YZ2分子的电子式是__________,该分子的空间构型是_____________。
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲中Y原子的杂化类型是_______,它能溶于水的原因是______________。
(5)金属F与XE的热浓溶液反应产物之一是X3[FE4],该反应的化学方程式是______________。
(6)F与Z形成的一种晶胞结构如图,其中F原子均匀地分散在立方体内部,原子a、b、d的坐标参数依次为(0,0,0)、(![]() ,
, ![]() ,
, ![]() )、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。
)、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明乙酸是弱酸的事实是
A. 乙酸和水能以任意比例混溶
B. 在稀乙酸水溶液中含有未电离的乙酸分子
C. 乙酸与Na2CO3溶液反应放出CO2气体
D. 1 mol·L-1的乙酸水溶液能使紫色石蕊溶液变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别只用一种试剂除去下列各组中所含的少量杂质(括号内为杂质),在空格中填上所需试剂的化学式:
(1)CO2(HCl) ______________,(2)FeSO4(CuSO4)_______,
(3)Fe2O3(Al2O3)___________,(4)Cu(Fe)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】方铅矿(主要成分是PbS,含少量ZnS、Fe、Ag)是提炼铅及其化合物的重要矿物,其工艺流程如下:

回答下列问题:
(1)流程中“趁热”过滤的原因是_____________,滤渣的主要成分是_________________。
(2)该工艺流程中可循环利用的物质是__________________。
(3)PbSO4与PbS在加热条件下发生反应的化学方程式为_____________________。
(4)《药性论》中有关铅丹(Pb3O4)的描述是:“治惊悸狂走,呕逆,消渴。”将PbO高温焙烧可制得铅丹,铅丹中含有的PbO与Al2O3性质相似,可用氢氧化钠溶液提纯铅丹,提纯时发生反应的离子方程是_______________。
(5)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,电解过程中阳极的电极反应式为____________;若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池负极增重_____g。
(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中 =__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
=__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com