
 如图所示,在容器A、B中分别装有20℃的水50mL,试管C、D相连通,其中存在下列平衡:2NO2(g)?N2O4(g)△H=-57kJ/mol;当向A中加入2g苛性钠时:
如图所示,在容器A、B中分别装有20℃的水50mL,试管C、D相连通,其中存在下列平衡:2NO2(g)?N2O4(g)△H=-57kJ/mol;当向A中加入2g苛性钠时:| c(N2O4) |
| c2(NO2) |
| 0.06mol/L |
| 0.07mol/L |
| c(N2O4) |
| c2(NO2) |
| 0.03 |
| 0.01×0.01 |


科目:高中化学 来源: 题型:
| A、Ba2+、Na+、Cl-、SO42- |
| B、Ag+、Al3+、NO3-、H+ |
| C、Na+、HCO3-、Cl-、OH- |
| D、K+、H+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | |||||||||||||||||
| ③ | ④ | ⑤ | |||||||||||||||
| ② | ⑥ | ||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图,将铜片和锌片焊接在一起组成A极,B为碳棒,进行电解实验,电解液中含硝酸银和硝酸铜各0.1mol.已知电路中通过0.2mol 电子.
如图,将铜片和锌片焊接在一起组成A极,B为碳棒,进行电解实验,电解液中含硝酸银和硝酸铜各0.1mol.已知电路中通过0.2mol 电子.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-OH与OH-组成元素相同,含有的质子数也相同 |
B、NH4Cl的电子式为: |
C、丙烷分子的比例模型示意图: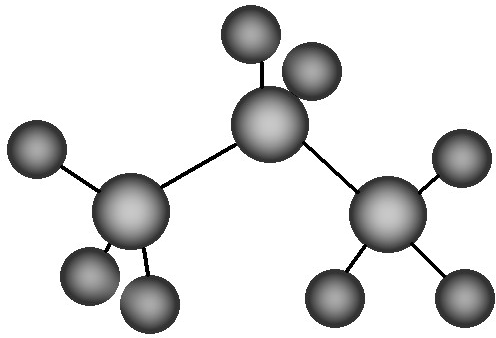 |
D、CO2分子的比例模型示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①>②>④>③ |
| B、②>③>④>① |
| C、①>②>③>④ |
| D、③>②>④>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com