
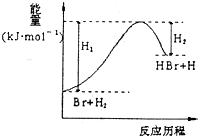
| A. | 正反应为吸热反应 | |
| B. | 加人催化剂,该化学反应的反应热改变 | |
| C. | 反应物总能量高于生成物总总量 | |
| D. | 升高温度可增大正反应速率,降低逆反应速率 |
分析 根据反应物的总能量小于生成物的总能量,可知反应吸热,
A、正反应为吸热反应;
B、催化剂与反应热无关;
C、正反应为吸热反应;
D、升高温度可增大正反应速率,也增大逆反应速率.
解答 解:根据反应物的总能量小于生成物的总能量,可知反应吸热.
A、反应物的总能量小于生成物的总能量,则正反应为吸热反应,故A正确;
B、催化剂只能降低反应所需的活化能,对反应热无影响,故B错误;
C、正反应为吸热反应,反应物总能量低于生成物总能量,故C错误;
D、升高温度,活化分子百分数增大,有效碰撞几率增大,反应速率增大,则可增大正反应速率,也增大逆反应速率,故D错误;
故选A.
点评 本题考查反应热,要掌握反应物的总能量小于生成物的总能量,反应吸热,反应物的总能量大于生成物的总能量,反应放热,题目难度不大.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 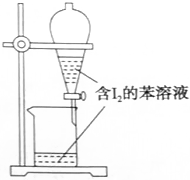 萃萃取碘水中的I2,分出水层的操作 | |
| B. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| C. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| D. | 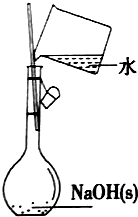 配制0.1mol•L-1的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | ⅡA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | D | F | |||||
| 3 | A | B | C | E |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
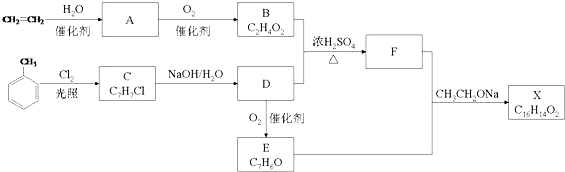

 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O
+2H2O 
 B.
B.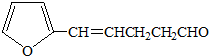
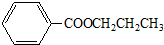
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素的金属性不一定比ⅡA族元素的金属性强 | |
| B. | VIA族元素的氢化物中,稳定性最好的是H2O | |
| C. | 同周期非金属元素最高价氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
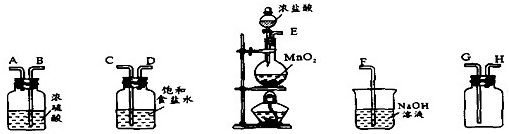
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com