
下列化工生 产过程中所发生的反应不属于氧化还原反应的是( )
产过程中所发生的反应不属于氧化还原反应的是( )
A.用氯气和消石灰制漂白粉 B.用氢气和氮气合成氨
C.用铝土矿冶炼金属铝 D.用油脂制肥皂
 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
下列关于金属的说法中,不正确的是( )
A.合金比纯金属具有较好的性能,硬度都比成分金属高,熔点比成分金属的低
B.在一般情况下,合金的硬度大于它的成分金属
C.常用电解法冶炼钠、镁、铝等活泼金属
D.将钢闸门与电源正极相连,可防止其在海水中被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
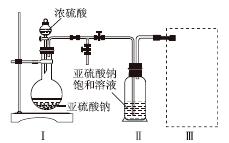
(1)装置Ⅰ中产生气体的化学方程式为______________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______。
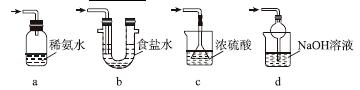
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO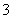 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
________________________________________________________________________
________________________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1CH3COONa溶液与0.1 mol·L-1HCl溶液等体积混合:
c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-)
B.0.1 mol·L-1NH4Cl溶液与0.1 mol·L-1氨水等体积混合(pH>7):
c(NH3·H2O)>c(NH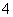 )>c(Cl-)>c(OH-)
)>c(Cl-)>c(OH-)
C.0.1 mol·L-1Na2CO3溶液与0.1 mol·L-1NaHCO3溶液等体积混合:
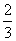 c(Na+)=c(CO
c(Na+)=c(CO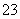 )+c(HCO
)+c(HCO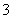 )+c(H2CO3)
)+c(H2CO3)
D.0.1 mol·L-1Na2C2O4溶液与0.1 mol·L-1HCl溶液等体积混合(H2C2O4为二元弱酸):
2c(C2O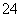 )+c(HC2O
)+c(HC2O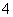 )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01 mol·L-1的X、Y、Z、W溶液的pH。
| 0.01 mol·L-1的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
(1)X、W的化学式分别为________、________。
(2)W在溶液中的电离方程式为________________________________________________________________________。
(3)25 ℃时,Z溶液的pH>7的原因是__________________________(用离子方程式表示)。
(4)将X、Y、Z各1 mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为____________________________________________。
(5)Z溶液与W溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为____________________________________________。
8.(1)NaOH NH4NO3
(2)NH4NO3===NH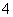 +NO
+NO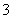
(3)NO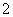 +H2O
+H2O
 HNO2+OH-
HNO2+OH-
(4)c(Na+)>c(NO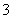 )>c(NO
)>c(NO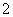 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
(5)NaNO2+NH4NO3===NaNO3+N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
氧化性:IO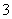 >Fe3+>I2
>Fe3+>I2
还原性:S2O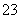 >I-
>I-
3I2+6OH-===5I-+IO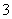 +3H2O KI+I2
+3H2O KI+I2 KI3
KI3
(1)取一定量某加碘盐(可能含有 KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化。 向试液中加足量KI固体,溶液显淡黄色,用 CCl4 萃取,下层溶液显紫红色。反应的离子方程式为________________、________________。
向试液中加足量KI固体,溶液显淡黄色,用 CCl4 萃取,下层溶液显紫红色。反应的离子方程式为________________、________________。
(2)KI 作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下KI 与氧气反应的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向某FeBr2溶液中,通入1.12 L(标准状况下)的Cl2,测得溶液中c(Br-)=3c(Cl-)=0.3 mol/L。反应过程中溶液的体积变化不计,则下列说法中正确的是( )
A.原溶液的浓度为0.1 mol/L
B.反应后溶液中c(Fe3+)=0.1 mol/L
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
日本冈山大学教授滨田博喜和研究员富良德等通过实验发现,桉树叶子的培养细胞能够消除有害化学物质双酚A的毒性。双酚A的结构简式如下图所示,下列有关此物质的说法正确的是( )
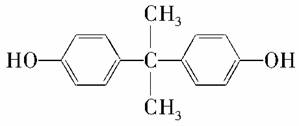
A.1 mol该物质与足量溴水反应消耗2 mol Br2
B.该物质能与碳酸氢钠溶液反应放出CO2
C.该物质的所有碳原子可能在同一平面
D.该物质与足量氢气发生加成反应后所得物质的化学式为C15H28O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能说明有机物分子中原子或原子团直接相连时而产生相互影响的是( )
A.苯酚能与NaOH溶液反应而乙醇不能
B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多
C.苯与液溴在铁作催化剂下发生反应,而苯酚与浓溴水混合就能发生反应
D.甲苯能使酸性高锰酸钾溶液褪色而甲烷不能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com