
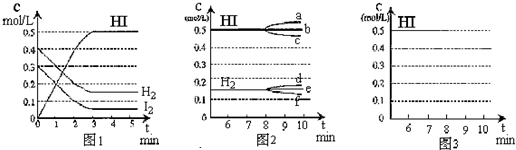
分析 (1)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算;
(2)由图象判断消耗氢气的量,可计算转化率;
(3)化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(4)若H2(g)、I2(g)、HI(g)的起始浓度分别用amol•L-1、bmol•L-1、cmol•L-1表示,达到平衡时各组分的浓度和图1的平衡状态相同;
(5)①根据化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,生成物浓度增大,反之,若平衡逆向移动,化学平衡常数K减少,生成物浓度减少;
②若加入I2,平衡正向移动,H2浓度减少;
(6)反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小.
解答 解:(1)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K=$\frac{{c}^{2}(HI)}{c({H}_{2})c({I}_{2})}$,故答案为:K=$\frac{{c}^{2}(HI)}{c({H}_{2})c({I}_{2})}$;
(2)由图象可知达到平衡时生成0.5molHI,则消耗0.25molH2,H2(g)的转化率为$\frac{0.25mol}{0.4mol}×100%$=62.5%,
故答案为:62.5%;
(3)A.v正(H2)=2v逆(HI),正逆反应速率不等,没有达到平衡状态,故A错误;
B.反应前后气体的体积不变,故容器总压强不随时间改变不能作为判断是否达到化学平衡状态的依据,故B错误;
C.混合气体中C(I2)不变,可说明达到平衡状态,故C正确;
D.都是气体参加反应,质量不变,体积不变,则密度不变,不能判断是否达到平衡状态,故D错误.
故选C;
(4)若H2(g)、I2(g)、HI(g)的起始浓度分别用amol•L-1、bmol•L-1、cmol•L-1表示,达到平衡时各组分的浓度和图1的平衡状态相同,则HI转化为碘、氢气与初始量相同,应满足a+$\frac{c}{2}$=0.4、b+$\frac{c}{2}$=0.3,
故答案为:a+$\frac{c}{2}$=0.4、b+$\frac{c}{2}$=0.3;
(5)①该反应放热,升高温度,平衡逆向移动,化学平衡常数K减少,生成物浓度减少,故答案为:减小;c;
②若加入I2,平衡正向移动,H2浓度减少,故答案为:f;
(6)H2(g)+I2(g)?2HI(g),反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小,碘化氢浓度减小一半为0.25mol/L,画出的变化图象如图: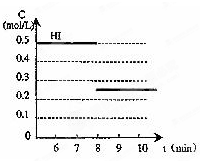 ,故答案为:
,故答案为: .
.
点评 本题主要考查了平衡常数、化学平衡移动以及化学反应速率的计算,为高考常见题型,难度较大,需要注意的是:化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,反之则减少.


科目:高中化学 来源: 题型:选择题
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 | |
| B. | 乙和甲中同种元素的质量分数相等,则乙能使湿润的KI淀粉试纸变蓝 | |
| C. | 丙中含有ⅣA族元素,则相同条件下丙比甲稳定 | |
| D. | 若丁分子空间构型为三角锥型,则丁分子间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H>0的反应一定不能自发进行 | |
| B. | 同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | |
| C. | 为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 | |
| D. | 硫酸工业中二氧化硫的催化氧化[2SO2(g)+O2(g)?2SO3 (g)],不采用高压是因为压强对SO2转化率无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6 | B. | 5 | C. | 4 | D. | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 经常使用一次性筷子、纸杯、塑料袋等做法能保护环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
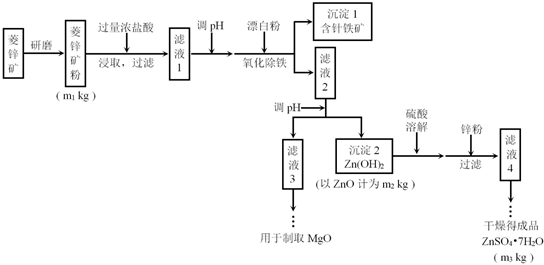
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | - | - |
| 沉淀完全的pH | 12.4 | 8.0 | - | - |
| 开始溶解的pH | - | 10.5 | - | - |
| Ksp | 5.6×10-12 | - | 6.8×10-6 | 2.8×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,它是由Na+与O22-(填写离子符号)构成的.
,它是由Na+与O22-(填写离子符号)构成的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “哑泉”之毒是由于水中的Cu2+使人体中的蛋白质分解 | |
| B. | “哑泉”之毒是由于水中的SO42-使人体中的蛋白质变性 | |
| C. | “哑泉”之毒是由于水中的Cu2+水解显酸性使人体中的蛋白质变性 | |
| D. | “安乐泉”能解“哑泉”之毒的离子方程式为Cu2++2OH-=Cu(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com