
 铝热反应实验如下:用两张圆形滤纸分别折叠成漏斗状,套在一起(先将置于内层的漏斗底部剪一个小孔,用水润湿),架在铁架台的铁圈上,下面放置盛沙的蒸发皿.将适量的炒干的氧化铁粉末和铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条,引燃氧化铁和铝粉的混合物,反应剧烈进行,发出耀眼的强光,生成铁和氧化铝.
铝热反应实验如下:用两张圆形滤纸分别折叠成漏斗状,套在一起(先将置于内层的漏斗底部剪一个小孔,用水润湿),架在铁架台的铁圈上,下面放置盛沙的蒸发皿.将适量的炒干的氧化铁粉末和铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条,引燃氧化铁和铝粉的混合物,反应剧烈进行,发出耀眼的强光,生成铁和氧化铝.分析 (1)①铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金;
②根据铝与NaOH溶液反应的性质设计实验方案;
③A.浓硫酸易使铁、铝钝化,不能使合金溶解;
B.活泼金属与稀硫酸反应;
C.稀硝酸与金属反应生成污染性气体;
D.铁不与NaOH溶液反应.
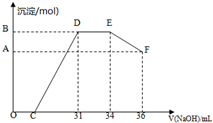
(2)①O→C 之间没有沉淀生成,说明硝酸过量,O→C 之间发生的反应酸碱中和反应,以此书写离子方程式;
②D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,以此书写离子方程式;根据反应顺序确定结合OH-的能力;
③B与A的差值为氢氧化铝的物质的量,由EF段消耗的氢氧化钠,根据Al(OH)3+OH-=AlO2-+2H2O,得出Al(OH)3的物质的量.
解答 解:(1)①铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金,所以铝热反应所得到的熔融物应是铁铝合金,
故答案为:合理;
②铝与NaOH溶液反应生成气体,反应的化学方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,所以可用NaOH溶液检验所得的块状熔融物中含有金属铝,
故答案为:NaOH溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑;
③A.浓硫酸易使铁、铝钝化,不能使合金溶解,故A错误;
B.活泼金属与稀硫酸反应,熔融物可溶解于稀硫酸中,故B正确;
C.稀硝酸与金属反应生成污染性气体,不是最佳选择,故C错误;
D.铁不与NaOH溶液反应,不能将熔融物全部溶解,故D错误;
故答案为:B;
(2)①O→C 之间没有沉淀生成,说明硝酸过量,O→C 之间发生的反应酸碱中和反应,离子方程式为H++OH-═H2O,
故答案为:H++OH-═H2O;
②D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,反应的离子方程式为:NH4++OH-═NH3•H2O;
上述现象说明溶液中最先结合OH-是氢离子,最后结合OH-是NH4+离子,所以溶液中的H+、Fe3+、Al3+离子结合OH-的能力强于是NH4+,
故答案为:NH4++OH-═NH3•H2O; H+;Fe3+;Al3+;NH4+;
③由图可知,EF段消耗的氢氧化钠溶液为36mL-34m=2mL,故该计算参加反应的氢氧化钠为0.002L×4mol/L=0.008mol,根据Al(OH)3+OH-=AlO2-+2H2O可知,Al(OH)3的物质的量为0.008mol,
故答案为:0.008.
点评 本题考查铝热反应、金属与硝酸的反应、离子方程式的书写、氧化还原反应、化学计算等知识点,题目难度较大,明确图中各阶段反应实质为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 容器内的原子总数不变 | B. | 容器内的分子总数不变 | ||
| C. | 容器内的压强保持不变 | D. | 容器内物质总质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液中水的电离程度小于Na2SO3 溶液,也小于Na2SO4 溶液 | |
| B. | [HSO3-]>[SO32-]>[H2SO3 ] | |
| C. | 该溶液中由水电离出的[H+]为1×10-4mol/L | |
| D. | 加入少量NaOH使溶液的pH升高会使水的电离受到抑制 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校化学课外活动小组设计如下图实验装置,完成探究某些物质的性质和比较性质强弱的实验.
某校化学课外活动小组设计如下图实验装置,完成探究某些物质的性质和比较性质强弱的实验.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .乙烯的电子式是
.乙烯的电子式是 .将6.72L(标准状况)乙烯和甲烷的混合气通入足量的溴水中,充分反应后,溴水的质量增加了1.4g,原混合气体中乙烯和甲烷的物质的量之比是1:5
.将6.72L(标准状况)乙烯和甲烷的混合气通入足量的溴水中,充分反应后,溴水的质量增加了1.4g,原混合气体中乙烯和甲烷的物质的量之比是1:5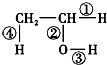 在不同的化学反应中会断裂不同的化学键,请写出下列反应的化学方程式,并指出反应时乙醇分子中断裂的化学键.
在不同的化学反应中会断裂不同的化学键,请写出下列反应的化学方程式,并指出反应时乙醇分子中断裂的化学键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 436kJ | B. | 557kJ | C. | 872kJ | D. | 181kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )| A. | X是NH3,Y是水 | B. | X是CO2,Y是饱和NaHCO3浓溶液 | ||
| C. | X是SO2,Y是NaOH溶液 | D. | X是HCl,Y是NaNO3稀溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ①⑤⑦ | C. | ③④⑤⑥ | D. | ②③④⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com