
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,加入足量氨水,振荡 | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①试管内壁有银镜生成 ②固态完全溶解,并有气体产生 | 假设3成立 |
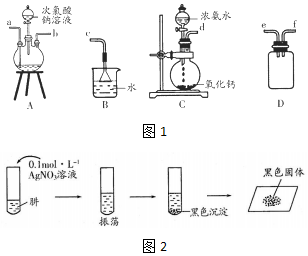
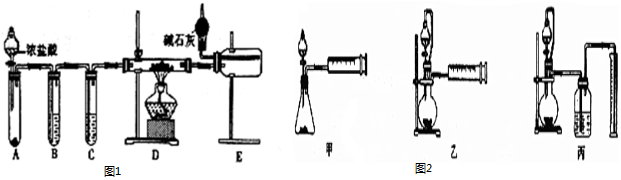
分析 (1)①实验室中用过量NH3和NaC1O溶液反应制取N2H4(液),装置C制备氨气,通过装置D防止倒吸,装置A中通入氨气和次氯酸钠溶液反应生成肼,最后通过装置B吸收剩余气体并防止倒吸;
②装置A中发生反应是次氯酸钠和氨气反应生成肼、氯化钠和水;装置D的作用是安全瓶;
(2)证明黑色沉淀已洗涤干净的操作是验证是否含银离子;
依据假设1、3得到假设2;
N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水,
实验编号1加入足量氨水,振荡银不溶;
操作同实验1加入足量氨水,黑色固体完全溶解说明为Ag2O;
①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热出现银镜反应;
②取少量黑色固体于试管中,加入足量稀硝酸,振荡黑色固体溶解证明含银;
假设1成立,则N2H4与AgNO3溶液反应生成银单质、氮气和水;
解答 解:(1)①实验室中用过量NH3和NaC1O溶液反应制取N2H4(液),装置C制备氨气,通过装置D防止倒吸,装置A中通入氨气和次氯酸钠溶液反应生成肼,最后通过装置B吸收剩余气体并防止倒吸,用图1装置制取肼,其连接顺序为:defabc,
故答案为:defabc;
②装置A中发生反应的化学方程式为:NaClO+2NH3=N2H4+NaCl+H2O,装置D的作用是安全瓶,防止倒吸的作用,
故答案为:NaClO+2NH3=N2H4+NaCl+H2O;防止倒吸或安全瓶;
(2)肼中加入硝酸银溶液,震荡得到黑色沉淀,证明黑色沉淀已洗涤干净的操作是检验是否存在硝酸银溶液,取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净,
故答案为:取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净;
假设1:黑色固体可能是Ag;
假设3:黑色固体可能是Ag和Ag2O,
得到假设2:黑色固体可能是Ag2O,
故答案为:Ag2O;
N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水.
实验编号1加入足量氨水,振荡银不溶;
操作同实验1加入足量氨水,黑色固体完全溶解说明为Ag2O;
①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热出现银镜反应;
②取少量黑色固体于试管中,加入足量稀硝酸,振荡黑色固体溶解,固态完全溶解,并有气体产生证明含银;
故答案为:
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 加入足量氨水,振荡 | 假设1成立 | |
| 2 | 假设2成立 | ||
| 3 | 试管内壁有银镜生成 固态完全溶解,并有气体产生 | 假设3成立 |
点评 本题考查了物质性质的实验验证、实验方案的设计和验证,综合性强,难度中等,解题需正确获取题干信息并能灵活运用所学化学知识,进行分析问题、解决问题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属Mg和金属Cu的空间利用率 | |
| B. | BF3和CH4中心原子的价层电子对数 | |
| C. | 邻羟基苯甲醛(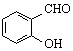 )和对羟基苯甲醛( )和对羟基苯甲醛(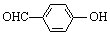 )的沸点 )的沸点 | |
| D. | C-O和Si-O的键能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F、Cl、Br、I最高正化合价都为+7 | |
| B. | 卤族元素的单质只有氧化性 | |
| C. | 从F到I,原子的得电子能力依次加强 | |
| D. | 卤素单质与H2化合的难易程度按F2、Cl2、Br2、I2的顺序由易变难 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下5.6L CH4含有的共用电子对数目为NA | |
| B. | 25℃时,pH=1的硫酸溶液中含有H+的数目为0.1NA | |
| C. | 常温下,23g NO2和N2O4混合气体中所含原子总数为1.5NA | |
| D. | 将0.5mol NH4NO3于稀氨水使溶液呈中性,溶液中NH4+数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ④⑥ | C. | ③⑥ | D. | ③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2 | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+=CaCO3 | |
| C. | 向H202溶液中滴加CuSO4溶液,产生气泡:2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2 T | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: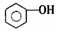 +CO32-→ +CO32-→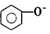 +HCO3- +HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
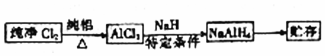
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com