
在热的稀硫酸溶液中溶解了11.4g硫酸亚铁固体,当加入50mL 0.5mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NxOy气体。
(1)推算出 x =_____;y =______。
(2)配平该反应的方程式:
__ FeSO4+ __ KNO3 +___H2SO4 — ____K2SO4 + ___Fe2(SO4)3 +____NxOy + ___H2O
(3)反应中氧化产物是_______________。
(4)用双线桥法表示该反应中的电子转移方向和数目??????:
_____________________________________________。
(1) 1 ; 1
(2)6 FeSO4+ 2 KNO3 +4H2SO4 = K2SO4 + 3Fe2(SO4)3 +2NxOy + 4H2O
(3)Fe2(SO4)3
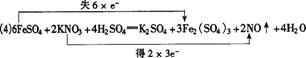
本题由得失电子守恒法求x和y。配平时先配后观察两步走。判断氧化剂或还原剂的方法是确定反应物和生成物在反应前后化合价的变化,化合价降低的反应物是氧化剂、化合价升高的反应物是还原剂。(1)n(FeSO4)=11.4g/152g·mol-1=0.075mol,KNO3的物质的量为0.05L×0.5mol·L-1=0.025mol,设NO3-与NxOy中N元素化合价差为a,根据得失电子总数相等的原则,可得关系式:0.075×1=0.025×a ,所以a=3即NxOy中N元素化合价为+2价,NxOy为NO ,所以x=y=1 (2)先配平氧化剂、还原剂、还原产物、氧化产物的化学计量数,再配平其他物质的化学计量数:6FeSO4+2KNO3+4H2SO4=3Fe2(SO4)3+K2SO4+2NO↑+4H2O (3)FeSO4中Fe元素失去电子,KNO3??中N元素得到电子,电子从铁元素向氮元素转移。电子总数为6e-,所以电子转移方向为FeSO4中Fe2+失e-,KNO3中氮得e-,故KNO3为氧化剂。还原剂为FeSO4,氧化产物是Fe2(SO4)3


科目:高中化学 来源: 题型:
 (2007?淄博三模)铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸.某化学研究小组在实验室中按下列步骤模拟该生产过程.填写下列空白:
(2007?淄博三模)铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸.某化学研究小组在实验室中按下列步骤模拟该生产过程.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
 对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.
对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
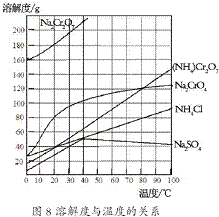 (2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:
(2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)过氧化钙是一种安全无毒的氧化物,通常含有部分CaO,且带有数量不等的结晶水。为分析某过氧化钙样品的组成,进行了如下实验。
① 称取0.270 g样品,灼热使之完全分解,生成CaO、O2和H2O,得到的O2在标准状况下体积为33.6 mL。
② 另取0.120 g样品,溶于稀盐酸,加热煮沸,使生成的H2O2完全分解。然后将溶液中的Ca2+ 完全转化为CaC2O4沉淀,经过滤洗涤后,将沉淀溶于热的稀硫酸,用0.0200 mol·L-1 KMnO4溶液滴定,共用去31.0 mL KMnO4溶液。化学方程式如下:
5CaC2O4+2KMnO4+8H2SO4 = K2SO4+2MnSO4+5CaSO4+10CO2↑+8H2O
(1) 写出CaO2受热分解的化学方程式。
(2) 计算样品中CaO2的质量分数。
(3) 计算样品中CaO2·x H2O的x值。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com