
| A. | 加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定含有SO42- | |
| B. | 观察钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,置于煤气灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察 | |
| C. | 待检液加入NaOH 溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+ | |
| D. | 取少量久置的Na2SO3 样品于试管中加水溶解,再加入足量盐酸有气体产生,然后加入BaCl2 溶液有白色沉淀产生,说明Na2SO3 样品已部分被氧化 |
分析 A.白色沉淀不一定为硫酸钡;
B.观察钾元素焰色反应应排除钠离子的干扰;
C.氨气为碱性气体,可使湿润的红色石蕊试纸变蓝;
D.加入足量盐酸有气体产生,然后加入BaCl2 溶液有白色沉淀产生,说明生成的沉淀不溶于盐酸.
解答 解:A.白色沉淀不一定为硫酸钡,不能检验硫酸根离子,应先加盐酸,再加氯化钡检验,故A错误;
B.观察钾元素焰色反应应排除钠离子的干扰,在灼烧的基础上透过蓝色钴玻璃进行观察,故B正确;
C.氨气为碱性气体,可使湿润的红色石蕊试纸变蓝,可说明原溶液中一定含有NH4+,故C正确;
D.加入足量盐酸有气体产生,说明含有Na2SO3,然后加入BaCl2 溶液有白色沉淀产生,说明生成的沉淀不溶于盐酸,可说明Na2SO3 样品已部分被氧化,故D正确.
故选A.
点评 本题考查常见离子的检验和鉴别,为高频考点,侧重于考查学生分析能力、实验能力,注意离子检验的试剂、现象及排除干扰离子,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 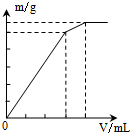 Al2(SO4)2 | B. | 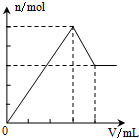 KAl(SO4)2 | C. | 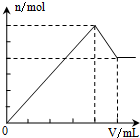 NH4Al(SO4)2 | D. | 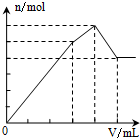 NH4Al(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
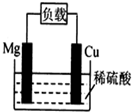
| A. | 电池反应为:Mg+2H+=Mg2++H2↑ | B. | 镁棒发生还原反应 | ||
| C. | 电子从铜棒经外电路流向镁棒 | D. | 铜棒为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
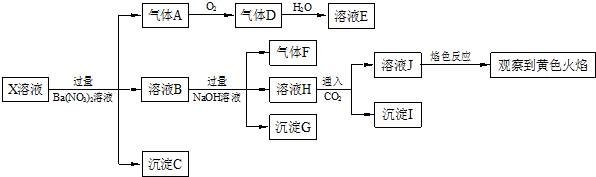
| A. | X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- | |
| B. | 气体F经催化氧化可直接生成气体D | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 | |
| D. | X中不能确定的离子是 A13+、Na+、K+和C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,负极质量增加 | |
| B. | 放电时,溶液中的BF4-向正极移动 | |
| C. | 充电时,阳极附近溶液的酸性增强 | |
| D. | 充电时,阴极的电极反应式为Pb2+-2e-═Pb |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是一种国际基本物理量 | |
| B. | 1 mol氢的质量为1g | |
| C. | 在同温同压下,相同体积的任何气体单质所含分子数相同 | |
| D. | 标准状况下气体摩尔体积约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-一定不能大量存在于该溶液中 | |
| B. | NH4+一定不能大量存在于该溶液中 | |
| C. | 该溶液的pH一定为12 | |
| D. | 该溶液中c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com