
 ①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是:2Zn+O2═2ZnO.则该电池的负极材料是锌;当导线中有1mol电子通过时,理论上消耗的O2在标准状况下的体积是5.6L.
①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是:2Zn+O2═2ZnO.则该电池的负极材料是锌;当导线中有1mol电子通过时,理论上消耗的O2在标准状况下的体积是5.6L.分析 ①负极发生氧化反应,锌失电子;根据1mol的锌失去2mol的电子进行计算;
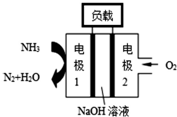
②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O,电池的总反应为4NH3+3O2=2N2+6H2O.
解答 解:①由反应2Zn+O2═2ZnO,锌发生氧化反应,所以锌是负极,当导线中有1mol电子通过时,理论上消耗的O2物质的量为:$\frac{1}{4}$mol,所以体积为:$\frac{1}{4}$mol×22.4L/mol=5.6L,故答案为:锌;5.6L;
②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O,电池的总反应为4NH3+3O2=2N2+6H2O,故答案为:2NH3+6OH--6e-═N2+6H2O;4NH3+3O2=2N2+6H2O.
点评 本题考查燃料电池的工作原理和规律:负极上是燃料失电子的氧化反应,在正极上氧气发生得电子的还原反应,比较容易.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与Cl2光照取代反应 | B. | 乙醇与浓硫酸共热 | ||
| C. | 乙炔在空气中的燃烧反应 | D. | 乙烯与氯化氢加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中各离子浓度大小关系c(Na+)>c(C2O42-)>c(OH-)>c(H+)>c(HC2O4-) | |
| B. | 若向溶液中不断加水稀释,水的电离程度增大 | |
| C. | 若用pH计测得溶液的pH=a,则H2C2O4的第二级电离平衡常数Ka2=1013-2a | |
| D. | 若向该溶液中加入等体积CaCl2溶液后能够产生沉淀,则CaCl2溶液的最小浓度应该大于2.4×10-8 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式: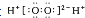 | B. | 次氯酸的结构式:H-O-Cl | ||
| C. | 中子数为10的氧原子:${\;}_8^{10}O$ | D. | 乙酸乙酯的结构简式:C4H8O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2SO4浓溶液和CuSO4溶液都能使蛋白质沉淀析出 | |
| B. | 苯中含有碳碳双键,其性质跟乙烯相似 | |
| C. | 乙烯使溴水褪色和苯与溴水混合振荡后水层变为无色原理相同 | |
| D. | 聚乙烯塑料的老化是由于发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
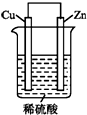 如图是Zn和Cu形成的原电池,回答下列问题:
如图是Zn和Cu形成的原电池,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
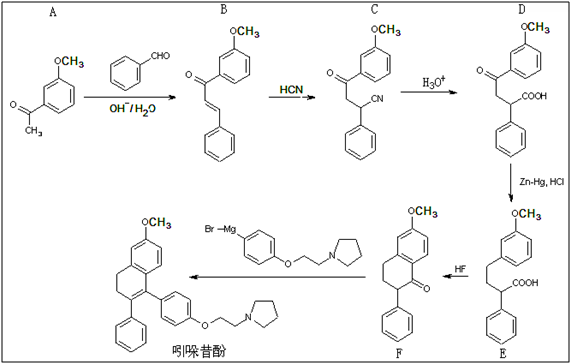 .
.
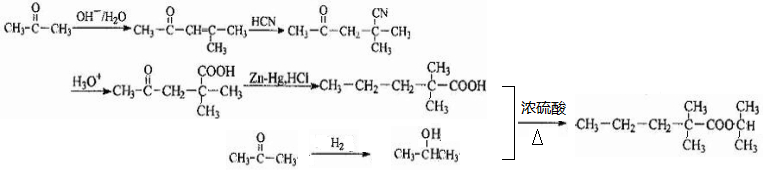 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com