
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:

(1)实验室灼烧海藻,需要下列仪器中的_____(填字母)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)提取碘的过程中,可选择的有机试剂是____(填字母)。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸
(3)小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈___色;他们打开分液漏斗下端的活塞,却未见液体流下,原因可能是_____。

【答案】cdef B 紫红 分液漏斗上口活塞小孔未与空气相通
【解析】
(1)根据灼烧固体的装置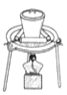 回答;
回答;
(2) 萃取剂必须具备下列条件:两种溶剂互不相溶;溶质在萃取剂中的溶解度大于在原溶剂中的溶解度;溶质与萃取剂不反应。
(3)碘易溶于CCl4,CCl4密度比水大;分液时,要打开分液漏斗上口玻璃塞和分液漏斗下端的活塞。
(1)根据装置 ,灼烧海带需要的仪器有:酒精灯、三脚架、泥三角及坩埚,故选cdef;
,灼烧海带需要的仪器有:酒精灯、三脚架、泥三角及坩埚,故选cdef;
(2)A.酒精和水互溶,所以酒精不能作萃取剂,故A错误;B.四氯化碳、苯符合萃取剂条件,所以能作萃取剂,故B正确;C.乙酸和水互溶,所乙酸不能作萃取剂,故C错误;答案选B;
(3)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,有机层在下方、水在上方,下层液体呈紫红色;如果分液漏斗上口玻璃塞未打开或分液漏斗上口活塞小孔未与空气相通,则液体不会流出。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①![]()
![]()
②![]()
![]()
③![]()
![]()
回答下列问题:
(1)反应![]() 的
的![]() =_________
=_________![]() 。
。
(2)在不同温度下,按照相同物质的量投料,发生反应①。测得CO的平衡转化率与“压强的关系如图1所示,下列说法正确的是________(填序号).
A.反应温度: ![]()
B.混合气体密度: ![]()
C.混合气体平均摩尔质量: ![]()
D.反应容器的体积关系: ![]()

(3)采用一种新型的催化剂(主要成分是Cu-Mn合金),利用CO和H2制备二甲醚(DME)。由图2可知,催化剂中![]() 约为______时最有利于二甲醚的合成。
约为______时最有利于二甲醚的合成。
(4)高温时二甲醚蒸气发生分解反应: ![]() 。迅速将二甲醚引人一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强p总如下表:
。迅速将二甲醚引人一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强p总如下表:

①该反应达到平衡状态时,二甲醚的转化率为___________。
②该反应的平衡常数Kp=_____。(用平衡分压代替平衡浓度计算,分压=总压X物质的量分数)
(5)一种以二甲醚作为燃料的燃料电池的工作原理如图3所示。其负极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
(氯化铁)熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
(氯化业铁)熔点为670℃,易升华。工业上采用向炽热铁粉中通人氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装詈(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为____。
(2)仪器D的名称是____;D中装的约品是碱石灰,其作用是____。
(3)定性分析。取C中的少量产物溶于稀盐酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的____(只能选取一种试剂,填序号)进行检测,实验现象是____。
①H2O2溶液 ②K3[Fe(CN)6]溶液 ③KSCN溶液
④酸性KMnO4溶液 ⑤KI一淀粉溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为____%(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施:
①用题目所给的装置制得的产物中,铁元素含量____(填“相等”、“偏高”或“偏低”),说明含有FeCl2杂质。
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1) ![]() 的系统命名为______________;
的系统命名为______________;
(2)3—甲基—2一戊烯的结构简式为______________;
(3)![]() 的分子式为______________;
的分子式为______________;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体
①试写出它的一种链式结构的同分异构体的结构简式______________.
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为______________形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型水系钠离子电池工作原理如图所示。TiO2光电极能使电池在太阳光照下充电,充电时Na2S4还原为Na2S,下列说法不正确的是

A. 充电时,太阳能转化为电能,电能又转化为化学能
B. 放电时,a极为负极
C. 充电时,阳极的电极反应式为3I――2e-=13-
D. M是阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. CO2与SO2 B. CH4与NH3 C. BeCl2与BF3 D. C2H2与C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】清晨,阳光射入密林中的现象如图。

请分析其中的化学道理,然后完成下列问题。
(1)图中的现象在化学上称作________,这说明森林中的空气具有________的性质。
(2)产生上述现象的根本原因是________________。
(3)此现象在化学上可用来____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. SO2 与 CO2 的分子立体构型均为直线形
B. H2O 和 NH3 中的中心原子杂化方式相同
C. CS2 为空间构型为 V 形的极性分子
D. HCN、SiF4 和 SO32- 的中心原子均为 sp3 杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com