
ĻÖÓŠ¼×”¢ŅŅĮ½øöŹµŃ飬½ųŠŠ·“Ó¦N2(g)+3H2(g) 2NH3(g)£»±ū”¢¶”Į½øöŹµŃ飬½ųŠŠ·“Ó¦H2(g)+I2(g)
2NH3(g)£»±ū”¢¶”Į½øöŹµŃ飬½ųŠŠ·“Ó¦H2(g)+I2(g)  2HI(g) ?H=-akJ?mol”Ŗ1,ŹµŃéĢõ¼žŗĶĘšŹ¼Ķ¶ĮĻČēĻĀ±ķĖłŹ¾£¬ŅŌĻĀ½įĀŪÕżČ·µÄŹĒ
2HI(g) ?H=-akJ?mol”Ŗ1,ŹµŃéĢõ¼žŗĶĘšŹ¼Ķ¶ĮĻČēĻĀ±ķĖłŹ¾£¬ŅŌĻĀ½įĀŪÕżČ·µÄŹĒ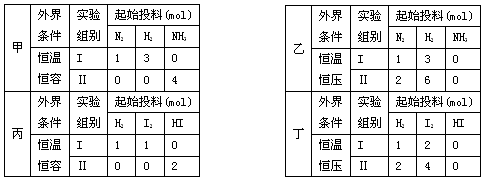
| A£®¼××éÖŠ£¬ČōĘ½ŗāŹ±N2ŗĶNN3µÄ×Ŗ»ÆĀŹ·Ö±šĪŖ¦Į1 ŗĶ¦Į2£¬Ōņ¦Į1 +¦Į2=1 |
| B£®ŅŅ×éÖŠ£¬Ę½ŗā¢ņÖŠNH3µÄÅØ¶ČŹĒĘ½ŗā¢ńµÄ¶ž±¶ |
| C£®±ū×éÖŠ£¬Čō“ļĘ½ŗāŹ±¢ńÖŠ·ÅČČQ1kJ, ¢ņÖŠĪüČČQ2kJ£¬ŌņQ1+Q2=a |
| D£®¶”×éÖŠ£¬“ļĘ½ŗāĖłŠčŹ±¼ä£ŗ¢ńŠ”ÓŚ¢ņ |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 £Ø2013?³ēĆ÷ĻŲŅ»Ä££©ĻÖÓŠĮ½·Żļ§ŃĪѳʷA”¢B£¬Ęä³É·Ö¶¼ŹĒ£ØNH4£©2SO4”¢NH4HSO4µÄ»ģŗĻĪļ£®¼×”¢ŅŅĮ½øöŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĻėŅŖČ·¶ØAŗĶBÖŠø÷³É·ÖµÄŗ¬Į森
£Ø2013?³ēĆ÷ĻŲŅ»Ä££©ĻÖÓŠĮ½·Żļ§ŃĪѳʷA”¢B£¬Ęä³É·Ö¶¼ŹĒ£ØNH4£©2SO4”¢NH4HSO4µÄ»ģŗĻĪļ£®¼×”¢ŅŅĮ½øöŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĻėŅŖČ·¶ØAŗĶBÖŠø÷³É·ÖµÄŗ¬Į森
| ||
| ||
| ŹµŃ鱹ŗÅ | ¢ń | ¢ņ | ¢ó | ¢ō |
| ļ§ŃĪµÄÖŹĮæ£Øg£© | 9.88 | 19.76 | 29.64 | 49.40 |
| ÅØĮņĖįŌö¼ÓµÄÖŹĮæ£Øg£© | m | m | 1.36 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠ¼×”¢ŅŅĮ½øöŹµŃ飬½ųŠŠ·“Ó¦N2£Øg£©+3H2£Øg£©?2NH3£Øg£©£»±ū”¢¶”Į½øöŹµŃ飬½ųŠŠ·“Ó¦H2£Øg£©+I2£Øg£©?2HI£Øg£©”÷H=-akJ?mol-1£¬ŹµŃéĢõ¼žŗĶĘšŹ¼Ķ¶ĮĻČēĻĀ±ķĖłŹ¾£¬ŅŌĻĀ½įĀŪÕżČ·µÄŹĒ£Ø””””£©
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ֊ѧ½Ģ²ÄČ«½ā””øßÖŠ»Æѧ±ŲŠŽ2£ØÅäɽ¶«æĘѧ¼¼Źõ³ö°ęÉēŹµŃé½ĢæĘŹé£© ɽ¶«æĘѧ¼¼Źõ³ö°ęÉēŹµŃé½ĢæĘŹé ĢāŠĶ£ŗ043
ĪŖĮĖ²ā¶ØŅ»ÖÖĘųĢ¬ĢžAµÄ»ÆѧŹ½£¬Č”Ņ»¶ØĮæµÄAÖĆÓŚŅ»ĆܱÕČŻĘ÷ÖŠČ¼ÉÕ£¬¶ØŠŌŹµŃé±ķĆ÷²śĪļŹĒCO2”¢COŗĶĖ®ÕōĘų£®ĻÖÓŠ¼×”¢ŅŅĮ½øö·½°øĄ“ĒóAµÄ×ī¼ņŹ½£®²āµĆµÄÓŠ¹ŲŹż¾ŻČēĻĀ(¼żĶ·±ķŹ¾ĘųĮ÷µÄ·½Ļņ£¬ŹµŃéĒ°ĻµĶ³ÄŚµÄæÕĘųŅŃÅž»)£ŗ
¼×£ŗ![]()
ŅŅ£ŗ![]()
ŹŌ»Ų“š£ŗ(1)ÄćČĻĪŖÄÄÖÖ·½°øÄÜĒó³öAµÄ×ī¼ņŹ½£¬¼ņŹöĄķÓÉ£®
(2)Ēėøł¾ŻÄćŃ”ŌńµÄ·½°ø£¬Ķعż¼ĘĖćĒó³öAµÄ×ī¼ņŹ½£®
(3)ČōŅŖČ·¶ØAµÄ·Ö×ÓŹ½£¬ŹĒ·ńŠčŅŖ²ā¶ØĘäĖūŹż¾Ż£æĖµĆ÷ĘäŌŅņ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğŗŚĮś½Ź”øßČż10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻÖÓŠ¼×”¢ŅŅĮ½øöŹµŃ飬½ųŠŠ·“Ó¦N2(g)+3H2(g)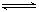 2NH3(g)£»±ū”¢¶”Į½øöŹµŃ飬½ųŠŠ·“Ó¦H2(g)+I2(g)
2NH3(g)£»±ū”¢¶”Į½øöŹµŃ飬½ųŠŠ·“Ó¦H2(g)+I2(g) 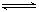 2HI(g) ∆H=-akJ•mol”Ŗ1,ŹµŃéĢõ¼žŗĶĘšŹ¼Ķ¶ĮĻČēĻĀ±ķĖłŹ¾£¬ŅŌĻĀ½įĀŪÕżČ·µÄŹĒ
2HI(g) ∆H=-akJ•mol”Ŗ1,ŹµŃéĢõ¼žŗĶĘšŹ¼Ķ¶ĮĻČēĻĀ±ķĖłŹ¾£¬ŅŌĻĀ½įĀŪÕżČ·µÄŹĒ
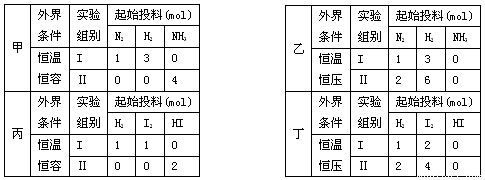
A£®¼××éÖŠ£¬ČōĘ½ŗāŹ±N2ŗĶNN3µÄ×Ŗ»ÆĀŹ·Ö±šĪŖ¦Į1 ŗĶ¦Į2£¬Ōņ¦Į1 +¦Į2=1
B£®ŅŅ×éÖŠ£¬Ę½ŗā¢ņÖŠNH3µÄÅØ¶ČŹĒĘ½ŗā¢ńµÄ¶ž±¶
C£®±ū×éÖŠ£¬Čō“ļĘ½ŗāŹ±¢ńÖŠ·ÅČČQ1kJ, ¢ņÖŠĪüČČQ2kJ£¬ŌņQ1+Q2=a
D£®¶”×éÖŠ£¬“ļĘ½ŗāĖłŠčŹ±¼ä£ŗ¢ńŠ”ÓŚ¢ņ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com