
A.v(N2)= 0.06 mol·L-1·min-1
B.v(Cl2)= 0.18 mol·L-1·min-1
C.v(HCl)= 0.024 mol·L-1·min-1
D.v(NH3)= 0.06 mol·L-1·min-1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 (2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.
(2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.| b×10-7 |
| a-b |
| b×10-7 |
| a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.溴化亚铁溶液中通入过量氯气:
Fe2++2Br+2Cl2![]() Fe3++Br2+4Cl-
Fe3++Br2+4Cl-
B.氯气通入冷的氢氧化钠溶液中:
2Cl2+2OH-![]() 3Cl-+ClO-+H2O
3Cl-+ClO-+H2O
C.向澄清石灰水中加入少量小苏打溶液:
Ca2++![]()
![]() CaCO3↓+H2O
CaCO3↓+H2O
D.氨水中通入过量二氧化硫:
2NH3·H2O+SO2![]() 2
2![]() +
+![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省烟台市高三3月诊断考试化学试卷(解析版) 题型:填空题
氮及其化合物在工农业生产中具有重要作用。
(1)某小组进行工业合成氨N2(g)+3H2(g)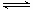 2NH3(g)
△H<0的模拟研究,在1L密闭容器中,分别加入0.1mol
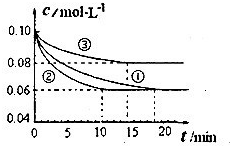
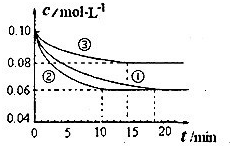
N2和0.3mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g)
△H<0的模拟研究,在1L密闭容器中,分别加入0.1mol
N2和0.3mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
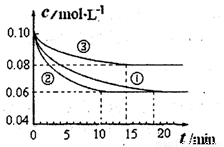
实验②从开始到达到平衡状态的过程中,用H2表示的平均反应速率为 。与实验①相比,.实验②所采用的实验条件可能为 (填字母),实验③所采用的实验条件可能为 (填字母)。
a.增大压强b.减小压强c.升高温度d.降低温度e.使用催化剂
(2)NH3可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+NO(g)+NO2(g)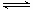 2N2(g)+3H2O(g) △H<0欲提高废气中氮氧化物的转化率,可采取的措施是
(填字母)
2N2(g)+3H2O(g) △H<0欲提高废气中氮氧化物的转化率,可采取的措施是
(填字母)
a.升高温度 b.增大压强 c,增大NH3的浓度
(3)NCl3遇水发生水解反应,生成NH3的同时得到 (填化学式)。ClO2是广谱高效消毒剂,制备原理为NCl3+6ClO2-+3H2O=NH3↑+6ClO2+3OH-+3Cl-。若转移1mol电子,则制取ClO2的质量为 。
(4)25℃时,将amol·L-1的氨水与bmol·L-1盐酸等体积混合,反应后溶液恰好显中性,则a b(填“>”、“<”或“=”)。用a、b表示NH3·H2O的电离平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮及其化合物在工农业生产中具有重要作用.
氮及其化合物在工农业生产中具有重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应离子方程式正确的是 ( )
A.大理石溶于醋酸溶液: CaCO3 + 2H+==Ca2+ + CO2 ↑+ H2O
B.氯气通入冷的氢氧化钠溶液中: 2Cl2 + 2OH- = 3Cl- + ClO-+ H2O
C.向澄清石灰水中加入少量小苏打溶液: Ca2+ + OH-+ HCO3- =CaCO3↓+ H2O
D.氨水中通入过量二氧化硫: 2NH3·H2O + SO2 = 2NH4+ + SO32-+ 2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com