
| A. | 实验室用无水乙醇加热至170℃,可制得乙烯 | |
| B. | 只用新制氢氧化铜悬浊液(可以加热)可将乙醇、乙醛、乙酸三种液体区别出来 | |
| C. | 用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸 | |
| D. | 将溴乙烷与NaOH溶液共热几分钟后冷却,滴入AgNO3溶液,观察沉淀颜色,不能用来检验溴乙烷中溴元素的存在 |
分析 A.乙醇应在浓硫酸催化下发生消去反应;
B.乙酸、乙醛和乙醇三种液体分别与氢氧化铜悬浊液混合,现象分别为蓝色溶液、砖红色沉淀、无现象;
C.乙酸乙酯不同于饱和碳酸钠溶液,乙酸可与碳酸钠反应;
D.检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有浅黄色沉淀生成.
解答 解:A.乙醇制取乙烯需要浓硫酸作催化剂,没有浓硫酸作催化剂不能制取乙烯,故A错误;
B.乙酸、乙醛和乙醇三种液体分别与氢氧化铜悬浊液混合,现象分别为蓝色溶液、砖红色沉淀、无现象,现象不同,可鉴别,故B正确;
C.乙酸乙酯不同于饱和碳酸钠溶液,乙酸可与碳酸钠反应,可用于除杂,故C正确;
D.将溴乙烷与NaOH溶液共热几分钟后冷却,加入硝酸酸化,滴入AgNO3溶液,观察沉淀颜色,可用来检验溴乙烷中溴元素的存在,故D正确.
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及知识点较多,把握常见有机物的性质及制备实验、混合物分离提纯等为解答的关键,注重高频考点的考查,题目难度中等.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验象 | 结论 |
| A | 将AlCl3溶液逐滴加NaOH溶液中 | 先无现象后产生白色胶状沉淀 | Al(OH)3是两性氢氧化物 |
| B | 向2支盛有醋酸和硼酸溶液的管中分别滴加Na2CO3溶液 | 醋酸:产生气泡; 硼酸:无现象 | Ka(CH3COOH)>Ka1(H2CO3)>Ka(H3BO3) |
| C | 将少量MgCl2溶液加入Fe(OH)3悬浊液中,振荡静置 | 沉淀由红褐色变为白色 | Fe(OH)3的溶解度大于Mg(OH)2 |
| D | 溴乙烷、乙醇及固体NaOH混合加热,产生的气态物质通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | 溴乙烷发生消去反应生成了乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| N≡N | H-H | N-H | |
| 键能数据(KJ/mol) | 946 | 436 | x |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 | |
| C. | MgCl2属于离子化合物,其中既含有离子键又含有共价键 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH | |
| B. | CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH | |
| D. | 2CH2=CH2+O2$→_{△}^{催化剂}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫离子(S2-)的核外电子排布式:1s22s22p63s23p6 | |
| B. | N2的结构式::N≡N: | |
| C. | NaCl的电子式: | |
| D. | CO2的分子模型示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方案 | 所选玻璃仪器 | |
| A | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 | 酒精灯、烧杯、玻璃棒 |
| B | 海带提碘 | 将海带剪碎,加蒸馏水浸泡,取滤液加稀硫酸和H2O2 | 试管、胶头滴管、烧杯、漏斗 |
| C | 测定饱和NaClO溶液、CH3COONa溶液的pH值 | 分别蘸取两种溶液滴在pH试纸上,颜色稳定后与标准比色卡对照 | 玻璃捧、玻璃片 |
| D | 配制480ml0.5mol/LCuSO4溶液 | 将称量好的 62.5g CuSO4•5H2O 溶解、冷却、转移、洗涤、定容、摇匀 | 烧杯、玻璃棒、量筒、一定规格的容量瓶、胶头滴管 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
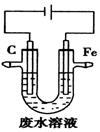
| A. | 石墨极上发生氧化反应 | |
| B. | 阳极的电极反应式为Fe-3e-=Fe3+ | |
| C. | 除去Cr2O72-的反应:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O | |
| D. | 随着电解的进行,石墨极附近电解质溶液的pH会减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com