
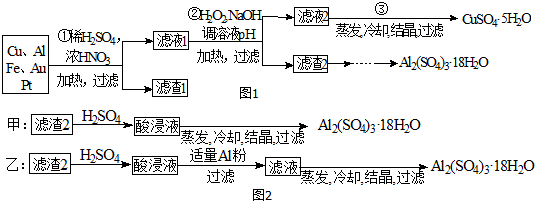
���� �����Ļ������ϡ���ᡢŨ�����Ϻ���ȣ�Cu��Al��Fe������Ӧ����Cu2+��Al3+��Fe2+����Au��Pt����Ӧ����������1 �ijɷ���Pt��Au����Һ1�е�������Cu2+��Al3+��Fe2+��Fe3+���ڢڲ���H2O2�������ǰ�Fe2+����ΪFe3+�������������ŵ��Dz��������ʣ�����Ի�������Ⱦ������ҺPH��Ŀ����ʹFe3+��Al3+�γɳ�����������Һ2�ijɷ���Cu2+���������ᾧ�ɵõ�CuSO4•5H2O���壬����2�ijɷ�Ϊ���������������������������м�H2SO4����Al2��SO4��3��Fe2��SO4��3�����������û�������������Һ��ֻ������������������ȴ���ᾧ�����˿ɵ����������壮
��1��ϡ���ᡢŨ�����������ȣ�Cu��Al��Fe������Ӧ����Cu2+��Al3+��Fe2+����������1 �ijɷ���Pt��Au��
��2��������������������ұ���ԭΪˮ������������Ⱦ������������������Ϊ���������ڳ�����ȥ��������ҺPHĿ���������Ӻ�������ȫ���������ڢڲ���H2O2�������ǰ�Fe2+����ΪFe3+�������������ŵ��Dz��������ʣ�����Ի�������Ⱦ������ҺPH��Ŀ����ʹFe3+��Al3+�γɳ�����������Һ2�ijɷ���Cu2+������2�ijɷ�Ϊ����������������������3������ʵ�鷽�����̷����Ʊ��������Ƿ������ʣ�ʹ�õ��Լ����ã�ԭ�ϵ������ʣ�ԭ�����������ط����жϣ�
��4�����ݵζ�ʵ��ͷ�Ӧ���ӷ���ʽ����õ����ζ�ʵ�����������ݱ���Һ���ĵĶ��ٽ��з����жϣ�
��� �⣺��1��ϡ���ᡢŨ�����������ȣ�Cu��Al��Fe������Ӧ����Cu2+��Al3+��Fe2+����������1�ijɷ���Pt��Au����Һ1�е�������Cu2+��Al3+��Fe2+���ڢٲ�Cu���ᷴӦ�����ӷ���ʽΪ��Cu+4H++2NO3-$\frac{\underline{\;\;��\;\;}}{\;}$Cu2++2NO2��+2H2O��Au��Pt�����Ӧ��������������
�ʴ�Ϊ��Au��Pt��
��2���ڢڲ���H2O2�������ǽ�Fe2+����ΪFe3+���������������������������ʣ��Ի�������Ⱦ��������ҺPH��Ŀ����ʹ�����Ӻ�������ȫ����������˵õ���������������������������Һ����ͭ��
�ʴ�Ϊ����Fe2+����ΪFe3+��Fe3+��Al3+��
��3���Ʊ�����������ļס������ַ����У�������������ֻ�����������������������������ȴ���ᾧ�����˵õ��������������л��д������������ʣ����������У��ҷ������������û�������������Һ��ֻ����������
�ʴ�Ϊ���ף����ò�Ʒ�к��н϶�Fe2��SO4��3���ʣ�
��4��ȡa g�������100mL��Һ��ÿ��ȡ20.00mL�������������Ӻ���c mol•L-1 EDTA��H2Y2-������Һ�ζ����յ㣬ƽ������EDTA��Һ6mL���ζ���Ӧ���£�Cu2++H2Y2-=CuY2-+2H+ͭ�������ʵ����ͱ�Һ���ʵ�����ͬ=cmol/L��b��10-3L=bc��10-3mol������Ԫ���غ�õ���
��20ml��Һ�к��е�CuSO4•5H2O���ʵ���Ϊbc��10-3mol��100ml��Һ�к�bc��10-3mol��5=5bc��10-3mol��
����CuSO4•5H2O���������ı���ʽ=$\frac{cmol/L��b��1{0}^{-3}L��250g/mol��5}{ag}$��100% ��
a��δ������ƿ��ʵ������Ӱ�죬��a����
b���ζ��յ�ʱ���ӵζ��ܶ���˵�����ı�Һ����ƫС�����ƫ�ͣ���b����
c��δ��������EDTA��Ӧ�ĸ������ӣ����ı�Һ�࣬���ƫ�ߣ���c��ȷ��
�ʴ�Ϊ��$\frac{cmol/L��b��1{0}^{-3}L��250g/mol��5}{ag}$��100%��c��
���� ����ͨ���Ʊ����������壬�������Ʊ�ʵ�鷽������ƣ������漰������������Ʊ����������ʵķ������ᴿ���к͵ζ��ļ�������ķ�������Ŀ�Ѷ��еȣ���ȷ�Ʊ�ԭ��Ϊ�����ؼ��������ֿ�����ѧ���ķ�����������������ѧʵ�顢��ѧ����������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��֪����N2��g��+O2��g��=2NO��g����H1=+180kJ•mol-1
��֪����N2��g��+O2��g��=2NO��g����H1=+180kJ•mol-1| A�� | ��Ӧ���е������仯����ͼ��ʾ�����H2=E1-E3 | |
| B�� | H2��ȼ����Ϊ241.8 kJ•mol-1 | |
| C�� | �ɷ�Ӧ��֪���¶�һ���������£���һ�����ܱ�������ͨ��1 mol N2��3 mol H2����Ӧ��ų�������ΪQ1 kJ����ͨ��2 mol N2��6 mol H2��Ӧ��ų�������ΪQ2 kJ����184.8��Q2��2Q1 | |
| D�� | ���Ĵ�������ӦΪ4NH3��g��+5O2��g��=4NO��g��+6H2O��g����H=+906 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ��Ӧ��Na+2H2O�TNa++OH-+H2�� | |
| B�� | ��������ͭ��Һ��Ӧ��Fe+Cu2+�TFe2++Cu | |
| C�� | ̼��������ᷴӦ��CO32-+2H+�TCO2��+H2O | |
| D�� | ����������Һ��ϡ���ᷴӦ��Ba2++SO42-�TBaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 28g��ϩ�������õ��Ӷ���ĿΪ4NA | |
| B�� | 1 mol����-CH3�������ĵ�������Ϊ9NA | |
| C�� | 0.5 mol1��3-����ϩ�����к���C=C˫����ΪNA | |
| D�� | ��״���£�11.2 L��������������Ϊ0.5 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Xn-��ԭ�Ӻ���һ���У�A-x-n�������� | |
| B�� | Xn-��ԭ�Ӻ���һ���У�x-n�������� | |
| C�� | Xn-�������һ������8�����ȶ��ṹ | |
| D�� | Xn-�Ĵ����һ���Ų���8������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
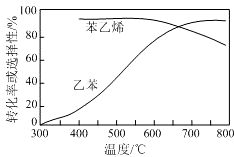 �ұ��������Ʊ���ϩ��Ӧ��
�ұ��������Ʊ���ϩ��Ӧ��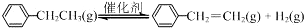
| ��ѧ�� | C-H | C-C | C=C | H-H |
| ����/kJ•mol?1 | 412 | 348 | 612 | 436 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����н������� | B�� | ����ǿ��ԭ�� | ||
| C�� | ��ɫ��Ӧ������ͬ | D�� | ���Ӳ�ṹ��ͬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com