
| A.除去NaCl溶液中的少量I2: 用无水乙醇,萃取分液 |
| B.除 CO2中的少量HCl:通入饱和Na2CO3溶液,洗气 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D.除去NaHCO3固体中的少量Na2CO3:加热灼烧 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
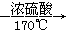 CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
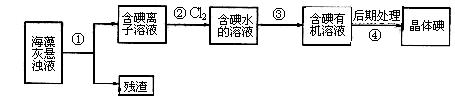
| A.步骤①、③的操作分别是过滤、萃取分液 |
| B.可用淀粉溶液检验步骤②的反应是否进行完全 |
| C.步骤③中加入的有机溶剂是乙醇 |
| D.步骤④的操作是过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲溶液含有SO42- | B.乙溶液含有SO42- |
| C.丙溶液显酸性 | D.丁溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A | A为0.1mol·L -1盐酸 | D为0.lmol·L-1NaCl溶液 | 老师评价:四位学生都及格,但是没有一个得满分 |
| B | A为0.1mol·L -1NaOH溶液 | C为0.1mol·L-1盐酸 | |
| C | A为1%酚酞 | B为0.1mol·L-1盐酸 | |
| D | D为0.1mol·L-1盐酸 | B为0.1mol·L-1 NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
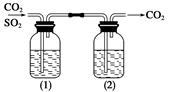
| A.(1)NaOH;(2)浓H2SO4 | B.(1)浓H2SO4;(2)NaOH |
| C.(1)NaHCO3;(2)浓H2SO4 | D.(1)浓H2SO4;(2)Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
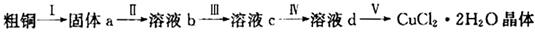
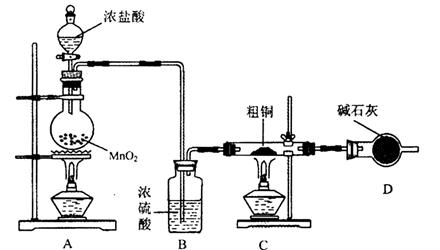
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
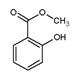 )具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸(
)具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸(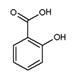 )与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )
)与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )| A.NaHCO3溶液 | B.NaOH溶液 | C.Na2CO3溶液 | D.NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com