
| A. | 氨气通入稀硫酸 NH3+H+═NH4+ | |
| B. | 稀烧碱溶液和氯化铵溶液混合 NH4++OH-═NH3•H2O | |
| C. | 碳酸氢铵和足量浓烧碱溶液混合加热 NH4++OH-═NH3↑+H2O | |
| D. | Cl2和水反应 Cl2+H2O═H++Cl-+HClO |
分析 A.氨气和稀硫酸反应生成硫酸铵;
B.稀氢氧化钠溶液和氯化铵反应生成氯化钠和一水合氨;
C.碳酸氢铵和足量浓氢氧化钠溶液混合加热,生成碳酸钠、氨气和水;
D.氯气和水反应生成盐酸和次氯酸.
解答 解:A.氨气和稀硫酸反应生成硫酸铵,离子方程式为NH3+H+=NH4+,故A正确;
B.稀氢氧化钠溶液和氯化铵反应生成氯化钠和一水合氨,离子方程式为NH4++OH-=NH3•H2O,故B正确;
C.碳酸氢铵和足量浓氢氧化钠溶液混合加热生成碳酸钠、氨气和水,离子方程式为NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$CO32-+H2O+NH3↑,故C错误;
D.氯气和水反应生成盐酸和次氯酸,离子方程式为Cl2+H2O?H++Cl-+HClO,故D正确;
故选C.
点评 本题考查了离子方程式的书写,明确离子方程式书写规则及发生的反应是解本题关键,注意BC选项的区别,掌握基础是解题关键,题目难度中等.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同物质的量浓度的NaA、HA混合溶液呈碱性 | |
| B. | 提高CO2兖气压力,碳酸饮料中c (A-)减小 | |
| C. | 当碳酸饮料的pH为5.0时,$\frac{c(HA)}{c({A}^{-})}$=0.16 | |
| D. | 碳酸饮料中各粒子的浓度关系为c( H+)=c( HCO3-)+2c( CO32-)+c(OH-)-c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 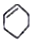 属于芳香族化合物 属于芳香族化合物 | B. | 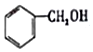 属于酚类化合物 属于酚类化合物 | ||
| C. | 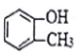 属于脂环化合物 属于脂环化合物 | D. | CH3CH2CH(CH3)2属于链状化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
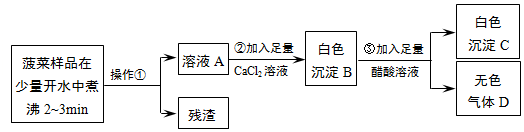
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不含OH-的溶液 | B. | 使酚酞试剂呈无色的溶液 | ||
| C. | pH=7的溶液 | D. | c(H+)=$\sqrt{{K}_{w}}$的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K-、Ba2+、NO3-、SO32- | B. | NH4+、Al3+、Cl-、SO42- | ||
| C. | K Na2+[Al(OH)4]-、SO42- | D. | Na+、K+、SO42-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④⑥ | C. | ①④⑤ | D. | ②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com