
【题目】3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥标明该反应中电子的转移及数目:___。
(2)还原剂是___;还原产物是___;被还原与未被还原N的个数比为___。
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
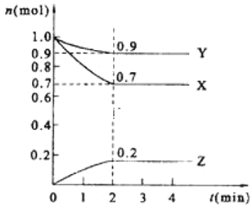
(1)由图中所给数据进行分析,该反应的化学方程式为___;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=___;
(3)当反应进行了3 min,该反应是否达到平衡___(填是或否);
(4)____时间段正逆反应速率相等;
(5)平衡体系中Y的百分含量(体积比)为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学。
(1)煤、石油和______称为化石燃料,燃煤(含杂质硫、氮等)造成的主要环境问题有______(答出一点即可)。
(2)请写出“加碘盐”中加入的碘酸钾(化学式为KIO3)中碘元素的化合价为_________
(3)扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉。其灭火原理是_________。
(4)治疗胃酸过多的药物中常含有Al(OH)3,试用化学方程式表示其治疗原理_____________
(5)下列净化水的过程中,说法不正确的是_________(填字母).
A.活性炭可吸附水中的色素和有异味的物质
B.明矾可以使硬水转化为软水
C.自来水厂净化水的方法主要有沉淀、过滤、吸附、消毒杀菌
D.净水方法中,净化程度最高的是蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() (b)、
(b)、![]() (d)、
(d)、![]() (p)的分子式均为C6H6,下列说法正确的是( )
(p)的分子式均为C6H6,下列说法正确的是( )
A. b的同分异构体只有d和p两种
B. b、d、p中只有b的所有原子处于同一平面
C. b、d、p均可与酸性高锰酸钾溶液反应
D. b、d、p的二氯代物均只有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.氢氧化钠的摩尔质量是40 g
B.1 mol NaOH的质量是40 g/mol
C.1 g H2和1 g N2所含分子数相等
D.等物质的量的N2、CH4、CO、H2O中,所含分子数一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铬盐厂生产过程中排出含Cr2O72-的工业酸性废水。为防止污染环境,现采用下列工艺流程进行处理后再排出。
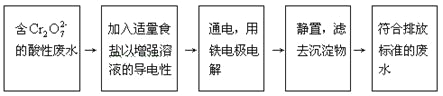
在整个处理过程中,Cr2O72-被还原为Cr3+,溶液的pH值逐渐升高,最后滤出的沉淀有Cr(OH)3和Fe(OH)3,试分析这个污水处理过程,回答:
(1)电解时,铁电极上的电极反应式:
阳极:__________________________________,
阴极:__________________________________。
(2)用铁(而不用炭)作电极进行电解的原因:__________________________。
(3)Cr2O72-在酸性环境中被还原剂还原,能除去Cr2O72-。减少溶液酸性是整个工艺流程中关键的一步,这个变化的离子方程式是____________。
(4)溶液的pH值逐渐增大的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由1~18号元素中部分元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)

请回答下列问题:
(1)物质A的化学式为____,其阴、阳离子个数比为____。
(2)化合物E溶于水中的电离方程式为____。
(3)实验室将物质C通常保存在____中,请写出反应①的离子方程式,并用单线桥标出电子转移的方向和数目____。
(4)反应②的化学方程式为____。
(5)有两个分别装有H和I固体的试剂瓶,因标签脱落而无法区分。若让你鉴别它们,下列试剂或方法中可选用的有____。
A 澄清石灰水 B 稀盐酸 C 加热,称重 D 焰色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________,其三种元素的电负性由小到大的顺序为______________。与COCl2互为等电子体的分子和离子(各写一种)__________。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______。

(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________(选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______g/cm3。(列出计算式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com