
����Ŀ��25��ʱ����c��CH3COOH��+c��CH3COO����=0.1 molL��1��һ����ᡢ�����ƻ����Һ����Һ��c��CH3COOH����c��CH3COO������pH�Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ����������ȷ���ǣ�������

A. �����ͼʾ�����25��ʱ����ĵ���ƽ�ⳣ��Ka=10��4.75
B. W������ʾ����Һ�У�c��Na+��+c��H+��=c��CH3COOH��+c��OH����
C. pH=3.5����Һ�У�c��Na+��+c��H+����c��OH����+c��CH3COOH��=0.1 molL��1
D. ��W������ʾ��1.0 L��Һ��ͨ��0.05 molHCl���壨��Һ����仯�ɺ��ԣ���c��H+��=c��CH3COOH����+c��OH����
���𰸡�D
�����������������A��W��c��CH3COOH����c��CH3COO-����ƽ�ⳣ��K =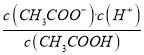 = 10-4.75molL-1��A��ȷ��B����Һ���ڵ���غ㣬ӦΪc��Na + �� + c��H + �� = c��CH3COO-�� + c��OH-����W��ʱc��CH3COOH����c��CH3COO-������c��Na������c��H���� �� c��CH3COOH����c��OH������B��ȷ��C���ɵ���غ㼰c��CH3COOH�� + c��CH3COO-�� = 0.1molL-1��֪��c��Na + �� + c��H + ��-c��OH-�� + c��CH3COOH�� = c��CH3COO-�� + c��CH3COOH�� = 0.1mol/L��C��ȷ��D����W������ʾ��Һ��ͨ��0.05molHCl���壬ԭ��ƽ�ⱻ���ƣ����������µ�ƽ�⣬��Һ�е���غ��ϵΪ��c��Na + �� + c��H + �� = c��CH3COO-�� + c��OH-�� + c��Cl-���������غ��ϵΪ��2c��Cl-�� = c��CH3COO-�� + c��CH3COOH�� = 0.1mol/L����2c��Na + �� + 2c��H + �� = 3c��CH3COO-�� + 2c��OH-�� + c��CH3COOH����c��Na + �� = 0.05mol/L��c��CH3COOH�� + c��CH3COO-�� = 0.1mol/L�����Ե�c��H + ���Tc��CH3COO-�� + c��OH-����D����ѡD��
= 10-4.75molL-1��A��ȷ��B����Һ���ڵ���غ㣬ӦΪc��Na + �� + c��H + �� = c��CH3COO-�� + c��OH-����W��ʱc��CH3COOH����c��CH3COO-������c��Na������c��H���� �� c��CH3COOH����c��OH������B��ȷ��C���ɵ���غ㼰c��CH3COOH�� + c��CH3COO-�� = 0.1molL-1��֪��c��Na + �� + c��H + ��-c��OH-�� + c��CH3COOH�� = c��CH3COO-�� + c��CH3COOH�� = 0.1mol/L��C��ȷ��D����W������ʾ��Һ��ͨ��0.05molHCl���壬ԭ��ƽ�ⱻ���ƣ����������µ�ƽ�⣬��Һ�е���غ��ϵΪ��c��Na + �� + c��H + �� = c��CH3COO-�� + c��OH-�� + c��Cl-���������غ��ϵΪ��2c��Cl-�� = c��CH3COO-�� + c��CH3COOH�� = 0.1mol/L����2c��Na + �� + 2c��H + �� = 3c��CH3COO-�� + 2c��OH-�� + c��CH3COOH����c��Na + �� = 0.05mol/L��c��CH3COOH�� + c��CH3COO-�� = 0.1mol/L�����Ե�c��H + ���Tc��CH3COO-�� + c��OH-����D����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������������NaCl��NaI��NH4Cl��Na2CO3��Na2SO3��Na2SO4�е�һ�ֻ�����ɣ�ȷ��ȡ4.7g�ù��������������ʵ�飨�����Լ����������������������ɱ�״������

����ʵ�����������й�˵������ȷ����
A. ԭ�����������Ƿ���NaC1��ȷ��
B. ԭ���������бغ���NH4Cl��Na2CO3��Na2SO3
C. �ⶨ������ɫ����3������������ȷ�����������
D. ����Һ1��ֻ��BaCl2�������ɰ�ɫ������������С��6.63g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ�������( )
A. ��Ba(OH)2��Һ�еμ�ϡ���Ba2����2OH����2H����SO![]() ===BaSO4����2H2O
===BaSO4����2H2O
B. ���Խ�����KMnO4����H2O2��2MnO![]() ��5H2O2��6H��===2Mn2����5O2����8H2O
��5H2O2��6H��===2Mn2����5O2����8H2O
C. �����ʵ�����MgCl2��Ba(OH)2��HCl��Һ��ϣ�Mg2����2OH��===Mg(OH)2��
D. Ǧ�����س��ʱ��������Ӧ��PbSO4��2H2O��2e��===PbO2��4H����SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���ڼӳɷ�Ӧ����
A.��ϩͨ������KMnO4��ҺB.�Ҵ���Ũ���Ṳ��
C.��Ȳʹ��ˮ��ɫD.���������������ˮ��Һ��ϼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ˮ�к���5.00��10-3mol/L��Cr2O72-���䶾�Խϴ�ij�о���ѧϰС��Ϊ�˱��Ϊ��������ˮ�����õ����Բ���Cr0.5Fe1.5FeO4������ͼʾ�����£�

�����й��жϴ������
A. �������з�Ӧ�����ӷ���ʽΪCr2O72-��6Fe2����14H��=2Cr3����6Fe3����7H2O
B. ���������õ������ɷ���ҪΪFe��OH��3��Fe��OH��2��Cr��OH��3
C. ���Բ���Cr0.5Fe1.5FeO4�У��ԣ�3�������ԣ�2����������֮��Ϊ2��3
D. ����ˮ�����ʲ����̷���Ӧ������1 L��ˮ�е�Cr2O72-��ȫת��ΪCr0.5Fe1.5FeO4��������������̷�13.9 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������������ء������й�˵��������ǣ�������
A.������ѧ���ʲ����ã�������ʳƷ������
B.ʯӢ�����õİ뵼����ϣ������Ƴɹ��أ�������ֱ��ת���ɵ���
C.����һ��Ӧ��ش�ţ��Ա��⵰���ʱ���
D.��ͥװ��ʱ��ˮ���������ͳ�������ᣬ�����ڽ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������ʵ�����Ϊ6.4 g������6.02��1022�����ӣ�����������Է���������
A. 64 B. 32 C. 96 D. 124
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.����Pt�����ʾ�����ԭ�ӵĶѻ���ʽ����ͼ����ʾ���侧����������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ����ͼ����ʾ��

��1����ͼ��֪���������岬�Ķѻ���ʽΪ_________��һ�������к���___����ԭ�ӣ�����ÿ����ԭ������ҵȾ���IJ�ԭ����_______����
��.��Ԫ�ص�һ�ֻ����PtCl2(NH3)2�����γ����ֹ��壬һ��Ϊ����ɫ����ˮ�е��ܽ�Ƚ�С����һ��Ϊ����ɫ����ˮ�е��ܽ�Ƚϴ���ش��������⣺
��2��PtCl2(NH3)2����ṹ��______________��
��3������ɫ������������___________���(�������Է����������Ǽ��Է�����)��
��4�����ֹ�����ˮ�е��ܽ��Բ��죬������____________ԭ�������ͣ�
��.̼����1��1-��������������ϲ�(��)�ļ�ƣ��ǵڶ������忹��ҩ����̼���ĽṹΪ��

��5����ѧ������ܶ࣬�磺�����Թ��ۼ������Ǽ��Թ��ۼ�������λ���������Ӽ��������������ަ������ߦ�����̼���к��е���������____������ĸ����
A���٢ڢۢޢ� B���٢ڢܢ� C���٢ۢݢ� D���ܢ�
��6����̼�������У�Cԭ�ӵ��ӻ���ʽ��_____ �֡�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com