
| n |
| V |
| 25g |
| 250g/mol |
| 0.1mol |
| 0.5L |
| 0.1L×0.2mol/L |
| 0.5L |


科目:高中化学 来源: 题型:
A、用铂作电极电解MgCl2溶液:2Cl-+2H2O
| ||||
B、用石墨电极电解氯化铜溶液:Cu2++2Cl-+2H2O
| ||||
C、向Ca(HCO3)2溶液中滴加少量的NaOH溶液:Ca2++HC
| ||||
| D、将少量氯气通入溴化亚铁溶液中:2Br-+Cl2═Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
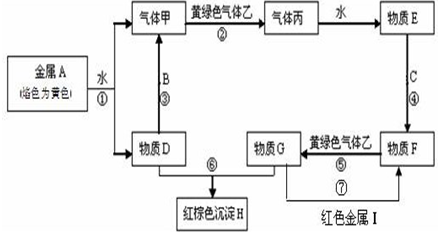 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 |
0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C、c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D、c(CO32-)>c(OH-)>c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在25℃时,向弱酸HAc中逐滴滴人NaOH溶液,在不同的pH下,HAc分子与Ac-离子的含量如图所示,则下列说法正确的是( )
在25℃时,向弱酸HAc中逐滴滴人NaOH溶液,在不同的pH下,HAc分子与Ac-离子的含量如图所示,则下列说法正确的是( )| A、当pH<2.6时,HAc不电离 |
| B、O点时.HAc恰好与NaOH完全反应 |
| C、pH=6.4时溶液中溶质只有NaAc |
| D、50℃,曲线交点O点pH<4.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、HCl溶液与NaOH溶液反应:H++OH-=H2O |
| C、石灰石溶于盐酸中:CO32-+H+=CO2↑+H2O |
| D、Zn与H2SO4溶液反应:Zn+2H+=Zn2++H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com