

分析 SnCl4极易水解,反应应在无水环境下进行进行,Ⅰ中发生反应:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,由于盐酸易挥发,制备的氯气中含有HCl及水蒸气,Ⅲ中试剂A为饱和食盐水除去HCl,可以降低氯气的溶解,浓硫酸吸收水蒸气,干燥氯气,氯气与Sn在Ⅳ反应生成SnCl4,未反应的氯气,用氢氧化钠溶液吸收,防止污染空气,干燥管中氯化钙吸收水蒸气,防止加入Ⅵ中使产物水解,以此解答该题.
解答 解:SnCl4极易水解,反应应在无水环境下进行进行,Ⅰ中发生反应:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,由于盐酸易挥发,制备的氯气中含有HCl及水蒸气,Ⅲ中试剂A为饱和食盐水除去HCl,可以降低氯气的溶解,浓硫酸吸收水蒸气,干燥氯气,氯气与Sn在Ⅳ反应生成SnCl4,未反应的氯气,用氢氧化钠溶液吸收,防止污染空气,干燥管中氯化钙吸收水蒸气,防止加入Ⅵ中使产物水解,
(1)氯气中混有氯化氢,应用饱和食盐水除去,则A为饱和食盐水,故答案为:饱和食盐水;
(2)Ⅰ中发生反应生成氯气,经过Ⅲ装置分别除去氯化氢、水蒸气,在Ⅳ中进行反应生成四氯化锡,经冷凝、回流,在Ⅵ中收集产物,最后连接干燥管,防止水解,则连接顺序为a→d→e→f→g→b→c→i→j→h,
故答案为:d→e→f→g→b→c→i→j;
(3)Ⅰ中发生反应:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(4)因金属锡易与氯气、氧气反应,反应时应先生成氯气,将氧气排出,则应点燃Ⅰ处酒精灯,
故答案为:Ⅰ;产生氯气,排出装置中的氧气,防止锡与氧气反应;
(5)因常温下,SnCl4遇水会发生剧烈反应,则Ⅴ可防止空气中的水蒸气进入装置Ⅵ,同时除去剩余的氯气,防止污染空气,
故答案为:防止空气中的水蒸气进入装置Ⅵ,同时除去剩余的氯气.
点评 本题考查制备实验方案设计、对原理与装置的分析评价、物质检验方案设计等,注意阅读题目获取信息并迁移运用,难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
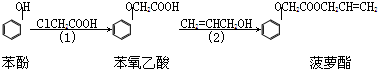
 (注明反应条件).
(注明反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成n mol O2的同时生成n mol NO2 | |
| B. | 单位时间内生成n mol O2的同时生成2n mol NO | |
| C. | 混合气体的密度不再改变的状态 | |
| D. | 混合气体的颜色不再改变的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据方程式回答相关问题:Fe+2HCl═FeCl2+H2↑
根据方程式回答相关问题:Fe+2HCl═FeCl2+H2↑查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和氢气 | B. | 氯气和溴 | C. | 铝和铁 | D. | 碳和硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯聚合为聚乙烯高分子材料 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 以铜和浓硝酸为原料生产硝酸铜 | D. | 用二氧化硅制备高纯硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
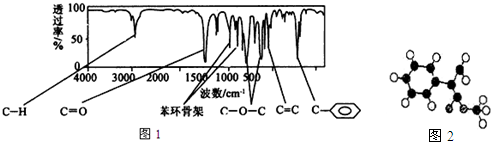
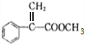 .
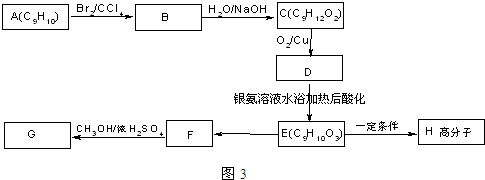
.
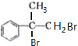 +2NaOH$→_{水}^{△}$
+2NaOH$→_{水}^{△}$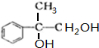 +2NaBr C→D
+2NaBr C→D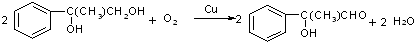 E→Hn
E→Hn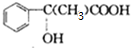 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(n-1)H2O
+(n-1)H2O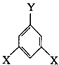 表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的四种物质的结构简式:
表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的四种物质的结构简式: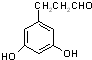 、
、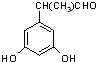 、
、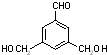 、
、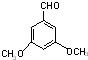 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
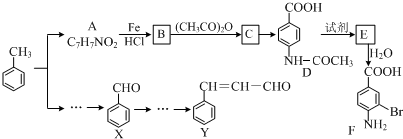
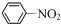 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$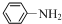
 +(CH3CO)2O→
+(CH3CO)2O→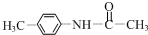 +CH3COOH.在合成F的过程中,B→C步骤不能省略,理由是氨基易被氧化,在氧化反应之前需先保护氨基.
+CH3COOH.在合成F的过程中,B→C步骤不能省略,理由是氨基易被氧化,在氧化反应之前需先保护氨基.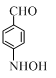 、
、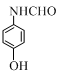 、
、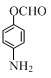 (写出3个).
(写出3个).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
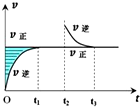
| A. | 该反应的Z和W-定不为气态 | |
| B. | t1-t2与t3-t4两时段,反应体系的气体平均摩尔质量不可能相等 | |
| C. | 该温度下,若此反应的平衡常数表达式为K=[X],则t1-t2与t3-t4两时段的c(X)相同 | |
| D. | 若在高温条件下,该反应才能自发进行,则该反应的平衡常数K随温度升高而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com