
| A. | 1.7 | B. | 2.0 | C. | 12.0 | D. | 11.7 |
分析 常温下,将0.1mol•L-1氢氧化钠溶液与0.06mol•L-1硫酸溶液等体积混合,先判断过量,然后计算过量的酸或碱的物质的量浓度,最后计算溶液的pH.
解答 解:常温下氢氧化钠溶液物质的量浓度为0.1mol/L,设溶液的体积都是1L,则氢氧化钠的物质的量为:1L×0.1mol•L-1=0.1mol,
硫酸的物质的量为:1L×0.06mol•L-1=0.06mol,含有H+的物质的量为0.06mol×2=0.12mol,
酸碱发生中和时H+和OH-的物质的量分别为0.12mol和0.1mol,则硫酸过量,过量的H+的物质的量为:0.12mol-0.1mol=0.02mol,
反应后溶液中H+的物质的量浓度为:c(H+)=$\frac{0.02mol}{2L}$=0.01 mol•L-1,
该混合液的pH=-lg10-2=2.0,
故选B.
点评 本题主要考查溶液pH的有关计算,题目难度中等,明确酸碱反应的过量分析是解答的关键,并应熟悉物质的量的计算、pH的计算公式来解答即可,试题培养了学生的化学计算能力.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 可逆反应的化学反应速率是指正反应速率 | |
| B. | 在可逆反应里正反应的速率是正值,逆反应的速率是负值 | |
| C. | 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度 | |
| D. | 对于可逆反应来说,反应物转化为生成物没有一定的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使石蕊试液变红 | |
| B. | 与铜反应生成Cu(NO3)2和NO气体 | |
| C. | 与Na2CO3反应放出CO2气体生成NaNO3 | |
| D. | 与C单质混合共热时生成CO2和NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
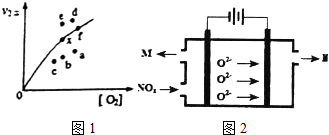
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业合成氨 | B. | 工业上用氨催化氧化法制备硝酸 | ||
| C. | 闪电导致雷雨中含有硝酸 | D. | 豆科植物的根瘤菌制造含氮化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层上电子数:A>B | D. | A的正价与B的负价的绝对值相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com