
【题目】某温度时,反应C(s)+H2O(g)![]() CO(g)+H2(g)在密闭容器中进行,下列条件的改变对其反应
CO(g)+H2(g)在密闭容器中进行,下列条件的改变对其反应
速率几乎无影响的是
A. 增加CO的量
B. 将容器的体积缩小一半
C. 保持体积不变,充入N2使体系压强增大
D. 保持压强不变,充入N2使容器体积变大
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25gmL﹣1、质量分数为36.5%的浓盐酸配制240mL 0.1molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为
(2)配制 240mL 0.1molL﹣1 的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次 ) .
A.用30mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12cm处
(4)若实验中遇到下列情况,对盐酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用于稀释盐酸的烧杯未洗涤, .
②容量瓶中原有少量蒸馏水, .
③定容时观察液面俯视, .
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度 .
②向容量瓶中转移溶液时有滚液不慎有溶液溅出 .
③定容摇勻后发现液面下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下图所示三套实验装置: 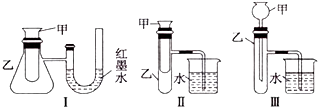
(1)图示3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 .
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里先加入适量氢氧化钡溶再加入稀硫酸,U形管中可观察到的现象 , 说明该反应属于(填‘吸热”或“放热”)反应.
(3)为探究固体M遇水的热效应,选择装罝Ⅱ进行实验,先在甲中放入适量的水,再加入M. ①若M为钠,则实验过程中烧杯中可观察到的现象是 .
②若只观察到烧杯里的玻璃管内形成一段水柱,则M可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F的原子序数逐渐增大,A和B同周期,A和F同族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的简单阴离子与C、D、E的简单阳离子电子层结构相同.请回答下列有关问题:
(1)F在元素周期表中的位置是 .
(2)C2B2的电子式是;AB2的结构式是 .
(3)B、C、D、E离子半径由大到小的顺序为(用离子符号回答); C、D、E最高价氧化物对应水化物的碱性由强到弱的顺序为(用化学式表示,且用“>”符号连接回答).
(4)C、E最高价氧化物对应水化物能够相互反应,则反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型锂-空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如右图所示,其中固体电解质只允许Li+通过。下列说法正确的是

A. 放电时,负极反应式:Li-e-+OH-=LiOH
B. 放电时,当外电路中有1 mol e-转移时,水性电解液离子总数增加NA
C. Li+穿过固体电解质向正极移动而得到LiOH溶液
D. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗11.2 L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2+3B2═2C的反应,在不同条件下的化学反应速率表示中,反应速率最快的是( )
A. v(A2)=0.4mol/(Ls) B. v(B2)=0.8mol/(Ls)
C. v(C)=0.6mol/(Ls) D. v(B2)=5.4mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的少量乙烯的操作方法是( )
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应CO(g)+H2O![]() CO2+H2 H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述错误的是( )
CO2+H2 H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述错误的是( )
A. 充入一定量的氮气,n(H2)不变 B. 减小压强,c(CO2)减小
C. 升高温度,![]() 减小 D. 更换高效催化剂,α(CO)增大
减小 D. 更换高效催化剂,α(CO)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com