
【题目】氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛。
(1)N2O是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生,此反应的化学方程式为___________。已知N2O与CO2分子具有相似的结构,试画出N2O的结构式_______。
(2)N2O4可作火箭高能燃料N2H4的氧化剂。
已知:2NO2(g)![]() N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;(a、b、c均大于0)。
写出气态腁在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式___________。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如p(NO2)=p总×x(NO2))。写出反应2NO2(g)![]() N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
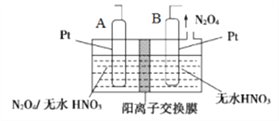
(4)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示。则电极B接直流电源的____极,电解池中生成N2O5的电极反应式为_____________。
(5)可用氨水吸收NO2、O2生成硝酸铵,写出该反应的离子方程式_____________。
已知25℃时NH3·H2O的电离常数Kb=2×10-5,向500ml0.1mol·L-1硝酸铵溶液中通入标准状况下至少____ml氨气,使溶液呈中性(溶液的体积变化忽略不计)。
【答案】NH4NO3![]() N2O↑+2H2ON=N=O2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H =-(c-a+2b)kJ·mol-1
N2O↑+2H2ON=N=O2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H =-(c-a+2b)kJ·mol-1![]() 负N2O4+2HNO3-2e-=2N2O5+2H+4NH3·H2O+4NO2+O2=4NH4++4NO3-+2H2O5.6
负N2O4+2HNO3-2e-=2N2O5+2H+4NH3·H2O+4NO2+O2=4NH4++4NO3-+2H2O5.6
【解析】(1)该反应中化合价变化为:NH4NO3→N2O,N元素由-3价→+1价,一个N原子失去4个电子,由+5价→+1价,一个N原子得4个电子,所以得失电子数的最小公倍数为4,所以硝酸铵的计量数为1,根据原子守恒确定另一种生成物为H2O,然后根据原子守恒配平其它元素,所以该反应的化学方程式为NH4NO3![]() N2O↑+2H2O ;模仿CO2的结构,N2O的结构式N=N=O ;
N2O↑+2H2O ;模仿CO2的结构,N2O的结构式N=N=O ;
(2)①2NO2(g)![]() N2O4(g) △H =-akJ·mol-1;②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;③N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;将①×(-1)+2×②—③依据盖斯定律得:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H =-(c-a+2b)kJ·mol-1 ;
N2O4(g) △H =-akJ·mol-1;②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;③N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;将①×(-1)+2×②—③依据盖斯定律得:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H =-(c-a+2b)kJ·mol-1 ;
(3)由题意p(NO2)=p总×x(NO2),p(N2O4)=p总×x(N2O4),2NO2(g)![]() N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式Kp=
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式Kp=![]()
(4)实验装置说明B电极上HNO3得电子产生N2O4,则电极B接直流电源的负极,电解池中生成N2O5的电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+ 。
(5)氧气将NO2氧化成HNO3,吸收氨气,4NH3·H2O+4NO2+O2=4NH4++4NO3-+2H2O;
25℃时NH3·H2O的电离常数Kb=2×10-5,向500ml0.1mol·L-1硝酸铵溶液中通入标准状况下氨气使溶液呈中性,依据电荷守恒计算可知,溶液中氢氧根离子浓度=10-7mol·L-1,c(NH4+)=c(NO3-),设混合后溶液体积为1L,(NH4+)=c(NO3-)=1mol·L-1;根据一水合氨电离平衡得到:NH3·H2O![]() NH4++OH-,平衡常数K=
NH4++OH-,平衡常数K=![]() ,c(NH3·H2O)=5×10span>-4mol/L,V(NH3)=5×10-4mol/L×0.5L×22.4mol/L=5.6×10-3L=5.6mL。
,c(NH3·H2O)=5×10span>-4mol/L,V(NH3)=5×10-4mol/L×0.5L×22.4mol/L=5.6×10-3L=5.6mL。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】常温下,将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L混合溶液,
(1)混合溶液中共有 种(填数字)不同的粒子。
(2)这些粒子中,浓度为0.01mol/L的是 ,浓度为0.002mol/L的是 。
(3)物质的量之和为0.01mol的两种粒子是__________________。
(4) 和 两种粒子数量之和比OH-多0.008mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
(1)x= 。
(2)平衡时C的浓度为多少?(要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类 ( )
A. 75%的酒精溶液 B. 硝酸钠 C. Fe(OH)3胶体 D. 豆浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中正确的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素aA、bB、cC、dD、eE的原子的结构示意图分别为
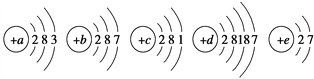
请回答下列问题:
(1)属于同周期的元素是__________(填元素符号,下同),属于同主族的元素__________。
(2)金属性最强的元素是__________,非金属性最强的元素是__________。
(3)上述元素中最高价氧化物对应的水化物碱性最强的是__________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有①Na+ 、②Ba2 +、③Cl一、④Br一、⑤SO32一、⑥SO42一 离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下。

下列结论正确的是( )
A. 肯定含有的离子是①④⑤ B. 肯定没有的离子是②⑥
C. 不能确定的离子是① D. 不能确定的离子是③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com