
| A、142g |
| B、71g |
| C、0.05mol |
| D、0.025mol |
科目:高中化学 来源: 题型:
| A、浓硝酸保存在玻璃塞的棕色试剂瓶中 |
| B、已经完成定容的500mL 1.0mol?L-1 的NaOH溶液,某同学不慎将容量瓶中溶液洒出,只能重新配制 |
| C、导管口点燃CO时需要验纯,H2加热还原CuO时也需要验纯 |
| D、物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| B、电镀时常采用镀层金属作阳极,镀件作阴极 |
| C、复合肥(如磷酸氢二铵)和生石灰能一起施用 |
| D、水的离子积常数K,随着温度的升高而增大,说明水的电离是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 |
| B、1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
| C、在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
| D、1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.21 mol?L-1 |
| B、0.56 mol?L-1 |
| C、0.24 mol?L-1 |
| D、0.12 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、SO3都是极性分子 |
| B、凡是中心原子采取sp3杂化轨道成键的分子其空间构型都是正四面体 |
| C、同周期ⅠA族元素和ⅦA族元素之间只能形成离子化合物 |
| D、干冰和氯化铵分别受热变为气体所克服的粒子间相互作用属于同种类型 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2的摩尔质量为32g |
| B、22.4LCO和H2的混合气体所含分子数为NA |
| C、0.1molN2和O2的混合气体在标准状况下的体积为2.24L |
| D、若1 molCO2所占体积为22.4L,则其所处状况一定为标准状况 |
查看答案和解析>>
科目:高中化学 来源: 题型:
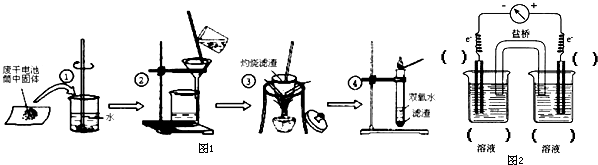
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com