
分子式为C4Hl0烷烃与氯气在光照条件下发生取代反应,生成物中含有两个氯原子且位于相邻碳原子上的同分异构体共有
A.3种 B.4种 C.5种 D.6种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015甘肃省天水市高二下学期第一次月考化学试卷(解析版) 题型:选择题
通过核磁共振氢谱可以推知(CH3)2CHCH2CH2OH有多少种化学环境的氢原子
A.6 B.5 C.4 D.3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市秦安县高三第一次模拟考试化学试卷(解析版) 题型:选择题
某有机物的结构简式如图所示,有关该物质的描述不正确的是

A.该物质的分子式为C11H12O3
B.该物质属于芳香族化合物
C.该物质能使溴水和酸性高锰酸钾溶液褪色,反应类型也相同
D.该物质在一定条件下反应能得到环状的酯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三第一次诊断考试理综化学试卷(解析版) 题型:填空题
(14分)工业上由焦炭或夭然气制氢气的过程中会产生一氧化碳。为了除去氢气中混有的一氧化碳,可在催化剂存在的条件下将一氧化碳与水蒸气发生反应:
CO(g)+H2O(g)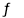 CO2(g)+H2(g) △H=-41.0 kJ·mol-l .
CO2(g)+H2(g) △H=-41.0 kJ·mol-l .
该反应在工业上被称为“一氧化碳变换”。
(1)写出该反应的平衡常数表达式:K= ;K ( 200℃ ) K ( 300℃ ) (填 “>”、“=”或“<”)。
(2)在773K时,一氧化碳发生反应的平衡常数K=9,如反应开始时CO和H2O的浓度都是0.020·mol-l ,则在此反应条件下一氧化碳的转化率为 。
(3)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数)。现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,以除去其中的CO。已知不同温度及反应物投料比(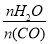 )下,变换后平衡混合气体中CO的体积分数如下表所示:
)下,变换后平衡混合气体中CO的体积分数如下表所示:
CO的体积分数/% 投料比 温度/℃ |
|
|
|
200 | 1.70 | 0.21 | 0.02 |
250 | 2.73 | 0.30 | 0.06 |
300 | 6.00 | 0.84 | 0.43 |
350 | 7.85 | 1.52 | 0.80 |
①从表中数据可以得到控制不同条件时CO的转化率的变化规律。能使CO的转化率升高,可改变的条件是 、 。
②温度是一氧化碳变换工艺中最重要的工艺条件,实际生产过程中将温度控制在300℃左右,其原因是 。
③温度为300℃、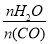 =1时,反应后的平衡混合气体中CO2的体积分数是 。(结果保留3位有效数字)o
=1时,反应后的平衡混合气体中CO2的体积分数是 。(结果保留3位有效数字)o
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:填空题
(16分)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
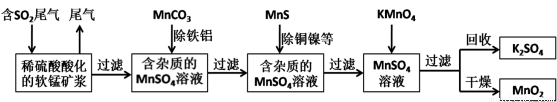
请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、 、 ;其中玻璃棒的作用是 。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是 。
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是 mol/L。
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式 。
(5)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液 d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过 (填操作名称)制得硫酸锰晶体(MnSO4H2O,相对分子质量为169)。已知废气中SO2浓度为8.4 g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000 m3燃煤尾气,可得到硫酸锰晶体质量为 kg(结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:选择题
下列有关物质性质的描述和该性质的应用均正确的是
A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏
B.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀
C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
D.二氧化锰具有较强的的氧化性,可作H2O2分解的氧化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:推断题
(16分)某抗抑郁药物有效成分F的合成路线如下:

回答下列问题:OR2 C11H9NO5 --H2O
(1)A的化学名称为 ;D分子中除一CHO外的含氧官能团结构简式为 ;
(2)E的结构简式为 ;反应①的反应类型为 ;
(3)反应B→C的化学方程式为 ;ClCH2COOC2H2加热条件下与足量NaOH反应后酸化所得有机物,发生聚合反应的化学方程式为 ;
(4)化合物C中含有苯环的同分异构体有 种,其中苯环上只有一个侧链且能发生银镜反应的有机物结构简式为 。
(5)下列有关F的叙述正确的是 。
a.分子式为C11H10O3N
b.既能与盐酸反应生成盐,也能在NaOH反应生成盐
c.1molF最多可以与2molH2反生加成反应
d.既能发生加扰反应也能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
(12分)稀土元素是周期表中ⅢB族钪、钇和镧系元素之总称,金属活泼性仅次于碱金属和碱土金属元素,它们的性质极为相似,常见化合价为+3价。无论是航天、航空、军事等高科技领域,还是传统工农业,稀土的应用几乎是无所不在。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
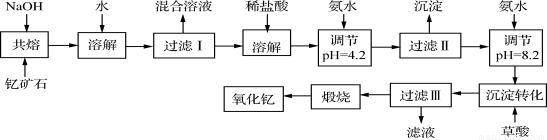
已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表。
离子 | 开始沉淀时 的pH | 完全沉淀时 的pH |
Fe3+ | 2.7 | 3.7 |
Y3+ | 6.0 | 8.2 |
②Be(OH)2+2NaOH  Na2BeO2+2H2O
Na2BeO2+2H2O
请回答下列问题:
(1)过滤Ⅲ所得滤液的溶质主要有______________。
(2)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用盐酸和________两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式 。
(3)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K= 。
Fe(OH)3+3H+的平衡常数K= 。
(4)写出煅烧过程的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com