
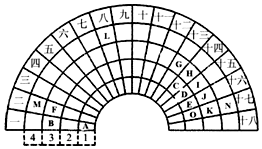
 Ԫ�����ڱ�����ʽ���ֶ�������ͼ������Ԫ�����ڱ���һ���֣�1��36��Ԫ�أ����Ա���ѧ����Ԫ�����ڱ���˼������Ԫ�����ڱ��������ɣ����ش��������⣺
Ԫ�����ڱ�����ʽ���ֶ�������ͼ������Ԫ�����ڱ���һ���֣�1��36��Ԫ�أ����Ա���ѧ����Ԫ�����ڱ���˼������Ԫ�����ڱ��������ɣ����ش��������⣺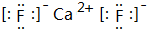 ���õ���ʽ��ʾCJ2���γɹ��̣�
���õ���ʽ��ʾCJ2���γɹ��̣�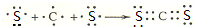 ��
������ ��Ԫ�������ڱ���λ�ÿ�֪��AΪ�⡢BΪNa��FΪMg��MΪCa��LΪFe��GΪAl��HΪ�衢CΪ̼��IΪ�ס�DΪ����JΪ��EΪ����NΪBr��KΪCl��OΪ����
��1���ɱ���֪��L�ڵ������ڵ�8�У�
��2�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ��
��3��MO2ΪCaF2���ɸ�����������ӹ��ɣ�CJ2ΪCS2��������Cԭ����Sԭ��֮���γ�2�Թ��õ��Ӷԣ���Cԭ�ӡ�Sԭ�ӵ���ʽ��ʾ���γɹ��̣�
��4��ͬ����������ҷǽ�������ǿ��ͬ������Ӳ�Խ��ǽ�����Խ��������������ۺ�����ǿ���Ʊ����������֤��
��5��A��E�γɵ�18�����ӵĻ�����ΪH2O2��A��J�γ�18�����ӵĻ�����ΪH2S�������������ǿ�����ԣ������������⣬��Ӧ����S��ˮ��
��� �⣺��Ԫ�������ڱ���λ�ÿ�֪��AΪ�⡢BΪNa��FΪMg��MΪCa��LΪFe��GΪAl��HΪ�衢CΪ̼��IΪ�ס�DΪ����JΪ��EΪ����NΪBr��KΪCl��OΪ����
��1���ɱ���֪��L�ڵ������ڵ�8�У������ڵ������ڵڢ��壻�ʴ�Ϊ���������ڵڢ��壻
��2�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶��P3-��Cl-��Ca2+��Mg2+��Al3+���ʴ�Ϊ��P3-��Cl-��Ca2+��Mg2+��Al3+��
��3��MO2ΪCaF2���ɸ�����������ӹ��ɣ������ʽΪ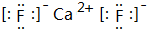 ��CJ2ΪCS2��������Cԭ����Sԭ��֮���γ�2�Թ��õ��Ӷԣ���Cԭ�ӡ�Sԭ�ӵ���ʽ��ʾ���γɹ���Ϊ��
��CJ2ΪCS2��������Cԭ����Sԭ��֮���γ�2�Թ��õ��Ӷԣ���Cԭ�ӡ�Sԭ�ӵ���ʽ��ʾ���γɹ���Ϊ��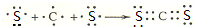 ��
��
�ʴ�Ϊ��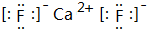 ��
��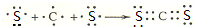 ��
��
��4��ͬ����������ҷǽ�������ǿ��ͬ������Ӳ�Խ��ǽ�����Խ�����ʷǽ�����C����S������������ۺ�����ǿ���Ʊ����������֤����Ӧ����ʽΪ��Na2CO3+H2SO4=Na2SO4+CO2��+H2O��
�ʴ�Ϊ������Na2CO3+H2SO4=Na2SO4+CO2��+H2O��
��5��A��E�γɵ�18�����ӵĻ�����ΪH2O2��A��J�γ�18�����ӵĻ�����ΪH2S�������������ǿ�����ԣ������������⣬��Ӧ����S��ˮ����Ӧ����ʽΪ��H2O2+H2S=2H2O+S����
�ʴ�Ϊ��H2O2+H2S=2H2O+S����
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ�ע����ս����ԡ��ǽ�����ǿ���Ƚϼ�ʵ����ʵ�������õ���ʽ��ʾ���ʻ�ѧ���γɣ���Ŀ�ѶȲ���


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2n+3m-a | B�� | m+2-a | C�� | n+m+a | D�� | m+2n+2-a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ṩ0.4 mol HCl��MnO2����������Ƶ�����4.48 L | |
| B�� | ���ṩ0.4 mol HCl��MnO2��������ת�Ƶ�����һ��Ϊ0.1mol | |
| C�� | ����0.4 mol HCl�μӷ�Ӧ������Ƶ�����2.24 L | |
| D�� | ����0.4 mol HCl������������Ƶ�����2.24 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | y���ʾ�Ŀ����ǵ����� | |
| B�� | y���ʾ�Ŀ����ǵ縺�� | |
| C�� | y���ʾ�Ŀ�����ԭ�Ӱ뾶 | |
| D�� | y���ʾ�Ŀ������γɻ�̬����ת�Ƶĵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ�����CH4�ڷ�Ӧ�١�����ת�Ƶĵ���������ͬ | |
| B�� | CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��l������H��-574kJ/mol | |
| C�� | 4NO2��g��+2N2��g���T8NO��g������H=+586kJ/mol | |
| D�� | ����2.24LCH4��NO2��ԭΪN2������������ת�Ƶĵ�������Ϊ0.8NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BeCl2��CO2 | B�� | H2O��SO2 | C�� | SO2��CH4 | D�� | NF3��CH2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com