
| A. | Al3+、Na+、NO3-、Cl- | B. | Fe3+、Na+、C1-、NO3- | ||
| C. | K+、NH4+、Cl-、AlO2- | D. | Cu2+、NH4+、SO42-、NO3- |
分析 常温下,pH=1的溶液呈酸性,离子之间不反应生成气体、沉淀、弱电解质或发生氧化还原反应、络合反应、双水解反应、和氢离子不反应的能大量共存,据此分析解答.
解答 解:常温下,pH=1的溶液呈酸性,
A.这几种离子之间不反应且和氢离子不反应,所以能大量共存,故A不选;
B.这几种离子之间不反应且和氢离子不反应,所以能大量共存,故B不选;
C.NH4+、AlO2-发生水解反应而不能大量共存,且AlO2-和氢离子反应而不能大量共存,故C选;
D.这几种离子之间不反应且和氢离子不反应,所以能大量共存,故D不选;
故选C.
点评 本题考查离子共存,为高频考点,侧重考查学生分析判断能力,明确离子性质及离子共存条件是解本题关键,题目难度不大,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | c(S2-)+c(HS-)+c(H2S)+c(H+)=c(OH-) | B. | c(OH-)=c(HS-)+c(H+)+2 c(H2S) | ||
| C. | c(Na+)=c(S2-)+c(HS-)+c(H2S) | D. | c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 25℃,1.01×105 Pa,64g SO2中含有的原子数为3NA | |
| B. | 在1mol的Na2O2晶体中离子总数为3NA | |
| C. | 在0.5mol/L NaCl溶液中,含有的Na+数目为0.5NA | |
| D. | 标准状况下,11.2LH2O 含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | 摩尔质量/(g•mol-1) | 质量/g | 物质的量/mol | 分子或离子数 |
| H2SO4 | 4.9 | |||
| SO2 | 0.5 | |||
| OH- | 6.02×1024 | |||
| NH4+ | 6.02×1022 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | 实验结论 | |
| 甲 | 在光照条件下,试管内气体颜色变浅了;试管内壁上出现了油状液滴. | CH4与Cl2在光照条件下 发生化学反应 |
| 乙 | 迅速剥开黑纸,立即观察,试管内气体颜色为黄绿色. | CH4与Cl2在无光照条件下不发生化学反应. |

 .
.

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
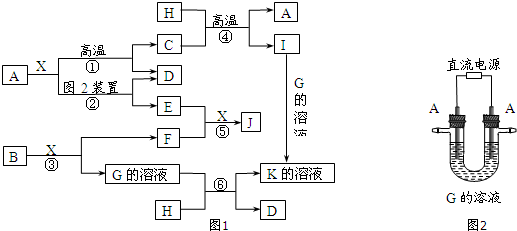
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com