
| 实验 |  | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色溶液 | |
| C | 无色 | 无色 | 白色沉淀 | 无色溶液 | |
| D | 红色 | 无色 | 白色沉淀 | 白色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
分析 二氧化硫为酸性氧化物,能够与氢氧化钠反应生成亚硫酸钠和水;具有漂白性,能够使品红褪色;具有还原性,能够被硝酸氧化生成硫酸根离子,硫酸钡离子与钡离子反应生成硫酸钡沉淀;二氧化硫与水反应生成亚硫酸,亚硫酸酸性弱于盐酸,所以二氧化硫与氯化钡溶液不反应,据此解答.
解答 解:二氧化硫为酸性氧化物,能够与氢氧化钠反应生成亚硫酸钠和水,所以a中溶液碱性减弱,颜色变为无色;
具有漂白性,能够使品红褪色,所以b中溶液变为无色;
具有还原性,能够被硝酸氧化生成硫酸根离子,硫酸钡离子与钡离子反应生成硫酸钡沉淀,所以C中产生白色沉淀;
二氧化硫与水反应生成亚硫酸,亚硫酸酸性弱于盐酸,所以二氧化硫与氯化钡溶液不反应,所以d中不会产生白色沉淀,
故选:C.
点评 本题考查了元素化合物,明确二氧化硫为酸性氧化物,具有漂白性、还原性的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 不能使酸性KMnO4溶液褪色 | B. | 该有机物中-OH能氧化为-CHO | ||
| C. | 能发生加成、取代、消去反应 | D. | 1mol该物质最多可与1molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44 | B. | 48 | C. | 64 | D. | 71 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 | |
| B. | 原电池的正极反应式为:O2十2H2O十4e-═4OH- | |
| C. | 电解后c(Na2CO3)不变,且溶液中有晶体析出 | |
| D. | 电池中c(KOH)不变;电解池中溶液pH变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl、HCl、NaOH、Cu | |
| B. | NaHCO3、液态H2SO4、Ba(OH)2、BaSO4液体 | |
| C. | 液氧、稀H2SO4、BaCl2、HNO3 | |
| D. | 酒精CO2、NH3、CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
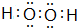 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com