
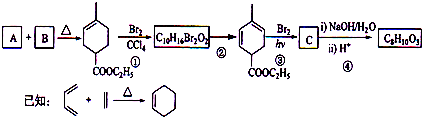
| A、发烟硫酸的摩尔质量为178 |
| B、反应①中氧化剂与还原剂的物质的量之比为2:3 |
| C、反应②中氧化产物与还原产物的物质的量之比为1:3 |
| D、若反应②中消耗2 mol I2(SO4)3,则电子转移3 mol |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、应量取的浓盐酸的体积是9.6mL |
| B、若开始时洁净的容量瓶中有少许蒸馏水,对实验没有影响 |
| C、量取浓盐酸时,仰视量筒将使所配溶液的浓度偏低 |
| D、定容摇匀后,发现液面低于刻度线,应立即加少量蒸馏水补齐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强酸性溶液中:Na+,Fe2+,Cl-,ClO- |
| B、加入Al能放出的H2溶液中:Cl-,HCO3-,NO3-,NH4+ |
| C、在由水电离出的c(OH-)=10-13mol?L-1的溶液中:Fe2+,Al3+,NO3-,Cl- |
| D、pH=11的溶液中:CO32-,Na+,[Al(OH)4]-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清透明溶液:Al3+、Na+、SO42-、HCO3- | ||
B、常温下
| ||
| C、能使酚酞变红的溶液:K+、NH4+、Cl-、NO3- | ||
| D、无色溶液:K+、Na+、SO42-、Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
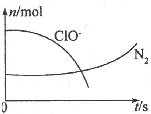 某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )| A、该反应的氧化剂是ClO- |
| B、消耗1 mol还原剂,转移3 mol电子 |
| C、氧化剂与还原剂的物质的量之比为2:3 |
| D、反应后溶液的酸性明显增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HY水解方程式为:HY-+H2O?Y2-+H3O+ |
| B、在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(OH-)>c(Y2-)>c(H+) |
| C、在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(Y2-)>c(H+) |
| D、H2Y 在电离时:H2Y+H2O?HY-+H3O+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com