
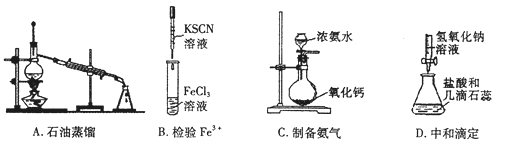
下列操作或仪器选用不正确的是
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:阅读理解
 用18mol/L的浓硫酸配制80mL 1.0mol/L的稀硫酸,需用的实验仪器有:A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
用18mol/L的浓硫酸配制80mL 1.0mol/L的稀硫酸,需用的实验仪器有:A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况,回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)Ⅰ.下列操作或仪器的选用正确的是
![]()

![]() Ⅱ.
Ⅱ.
Ⅱ. 某同学为了探究SO2与Na2O2的反应是否类似于CO2,设计反应装置见下图。
(1)选择制取SO2的合适试剂___________;
a.10%的H2SO4溶液 b.80%的H2SO4溶液 c.Na2SO3固体 d.CaSO3固体
(2)装置C中NaOH溶液的作用是________________;
(3)上述反应装置有些不足之处,为完善该装置,请从供选择的装置中选择需要的装置________(填编号,说明所选装置在整套装置中的位置___________________;
(4)移开棉花,将带火星的木条放在C试管口,木条不复燃,该同学认为SO2与Na2O2的反应不同于CO2,请据此写出反应的化学方程式_________________________;
(5)为检验是否有Na2SO4生成,设计如下方案
![]()

![]()
上述方案________(填“合理”、“不合理”),理由:______________________________;
![]()
(6)Na2O2反应完全后,为确定所得固体的组成,可进行如下操作:称取样品m g并溶于适量的水中,______________(选择下列操作的编号按操作顺序填入),烘干,称量,干燥沉淀质量为n g,计算含量。
a.加足量盐酸酸化的氯化钡溶液 b.加足量硫酸酸化的氯化钡溶液
c.过滤 d.洗涤 e.蒸发结晶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com