
| A. | 常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1mol | |
| B. | 一定条件下的可逆反应,反应物的转化率不可能达到100% | |
| C. | 沉淀溶解转换的实质是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动 | |
| D. | △H<0,△S>0的反应一定是自发进行的化学反应 |
分析 A、醋酸的分子数N=nNA,无体积只知道浓度无法判断;
B、可逆反应具有不完全性;
C、沉淀转化是向更难溶的方向进行;
D、△H-T△S<0的反应能够自发进行.
解答 解;A、pH=1的醋酸溶液中,氢离子浓度为0.1mol/L,醋酸的浓度一定大于0.1mol/L,但体积未知,无法确定醋酸的分子质的量,故A错误;
B、可逆反应具有不完全性,反应物的转化率不可能达到100%,故B正确;
C、沉淀转换的实质就是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动,故C正确;
D、△H-T△S<0的反应能够自发进行,△H<0,△S>0的反应一定能自发进行,故D正确;
故选A.
点评 本题考查可逆反应、反应的方向、沉淀转化等知识,难度不大,注意基础知识积累掌握.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:计算题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加H2O(g) 的量 | |
| B. | 增加C(s)的量 | |
| C. | 将容器的体积缩小一半 | |
| D. | 保持压强不变,充入N2,使容器的体积变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁制容器盛放硫酸铜溶液,容器易被腐蚀 | |
| B. | 利用催化措施,可以将汽车尾气中的CO和NO转化为无害气体 | |
| C. | 防止酸雨发生的重要措施之一是使用清洁能源 | |
| D. | 氧化铜呈红色,可作为制造陶瓷的红色颜料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
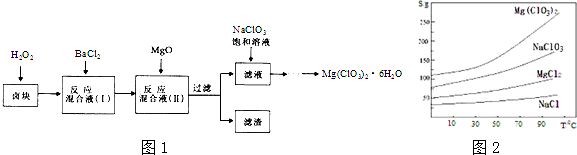
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
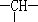 和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体)( )
和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体)( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 虽然固体氯化钠不能导电,但氯化钠是电解质 | |
| B. | 在纯水中加入少量硫酸铵,可抑制水的电离 | |
| C. | 在醋酸钠溶液中加入少量氢氧化钠,溶液中 c(OH-)增大 | |
| D. | 纯水的pH随温度的升高而减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com